题目内容
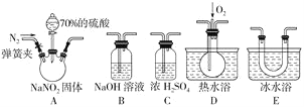
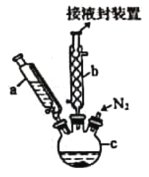
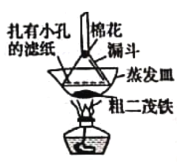
【题目】配制一定物质的量浓度的溶液,几个关键实验步骤和操作如图:

(1)现需要94 mL 0.10 mol·L-1 Na2CO3溶液,进行现场配制。上述实验步骤A~F正确的实验次序为_______________________(填字母)。步骤E中将一玻璃仪器上下颠倒数次,写出该仪器的名称_________________。
(2)步骤C通常称为溶解,步骤A通常称为_________。
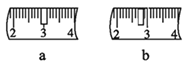
(3)用Na2CO3·10H2O来配制该溶液,托盘天平称取样品,游码需要打在图示________(填a或b)位置,若称量前晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏_______(填“大”或“小”或“无影响”)。
【答案】CBDFAE 100 mL容量瓶 定容 a 大
【解析】
本题考察一定物质的量浓度溶液配制,难度不大,考生运用所学知识答题即可。
(1)配制一定物质的量浓度溶液的操作步骤为:计算→称量→溶解→移液→洗涤→定容→摇匀→装瓶;上述实验步骤中,A为定容,B为移液,C为溶解,D为洗涤,E为摇匀,F为洗涤后的加水,故正确的实验次序为CBDFAE;E为容量瓶,由于要配制94mL的溶液,需要使用100mL的规格,故E为100mL容量瓶;
(2)A为定容;
(3)实验需要使用100mL容量瓶,则n(Na2CO3·10H2O)=0.1L×0.1mol·L-1=0.01mol,m(Na2CO3·10H2O)=0.01mol×286g·mol-1=2.9g,则需要用游码称0.9g,故选a;称量前晶体已经有一部分失去了结晶水,则称得的晶体中n(Na2CO3)偏大,故所配制的溶液浓度偏大。

 名校课堂系列答案
名校课堂系列答案【题目】下列除杂试剂或操作选用不正确的是( )
物质(括号内为杂质) | 除杂试剂或操作 | |
A | Na2CO3晶体(NaHCO3) | 加热 |
B | CO2(HCl) | 饱和氯化钠溶液、浓H2SO4,洗气 |
C | Fe2O3(SiO2) | NaOH 溶液,过滤 |
D | 稀盐酸(Cl2) | 光照 |
A.AB.BC.CD.D
【题目】与化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示)。下表是某温度下几种常见弱酸的电离平衡常数:
酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | 2×10﹣5 |
HClO | HClO | 3.0×10﹣8 |
H2CO3 | H2CO3 HCO3﹣ | K1=4.4×10﹣7 K2=5.61×10﹣11 |
H3PO4 | H3PO4 H2PO4﹣ HPO42﹣ | K1=7.1×10﹣3 K2=6.3×10﹣8 K3=4.2×10﹣13 |
回答下列问题:
(1)若把CH3COOH、HClO、H2CO3、HCO3﹣、H3PO4、H2PO4﹣、HPO42﹣都看作是酸,则它们酸性最强的是_______(填化学式,下同),最弱的是________。
(2)向NaClO溶液中通入少量的二氧化碳,发生的离子方程式为_______。
(3)求出该温度下,0.10molL﹣
(4)该温度下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定增大的是____。
A.c(H+) B.c(H+)c(CH3COO﹣) C.c(H+)c(OH﹣) D.c(OH﹣)/c(H+)
(5)取等体积的pH均为a的醋酸和次氯酸两溶液,分别用等浓度的NaOH稀溶液恰好中和,消耗的NaOH溶液的体积分别为V1,V2,则大小关系为:V1_____V2( 填“>”、“<”或“=”)。
(6)下列四种离子结合H+能力最强的是_______。
A.HCO3﹣ B.CO32﹣ C.ClO﹣ D.CH3COO﹣
(7)等物质的量的苛性钠分别用pH为2和3的醋酸溶液中和,设消耗醋酸溶液的体积依次为Va、Vb,则两者的关系正确的是(_________)
A.Va>10Vb B.Va<10Vb C.Vb <10 Va D.Vb>10Va