题目内容
【题目】在容积可变的密闭容器中充入2 mol A和1 mol B发生反应:mA(g) + nB(g) ![]() pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
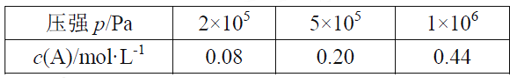
A. 维持压强2×105Pa,若反应开始后5min时达到平衡,则v(A)=0.016mol/(L·min)
B. P从2×105Pa增加到5×105Pa时,平衡逆向移动
C. P为1×106Pa时,平衡常数表达式K=![]()
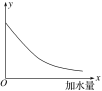
D. 其它条件相同时,在上述三个压强下分别发生该反应。A的转化率随时间变化曲线如图所示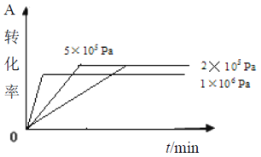
【答案】D
【解析】
由气体状态方程PV=nRT,得P=![]() RT即P=cRT,当温度相同时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,所以气体物质的计量数关系应为m+n=p。压强从5×105Pa增大到1×106Pa时,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol>0.4mol,浓度增大超过了2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面的分析,说明B在高压下变成液态或固体,由此分析解答。
RT即P=cRT,当温度相同时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,所以气体物质的计量数关系应为m+n=p。压强从5×105Pa增大到1×106Pa时,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol>0.4mol,浓度增大超过了2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面的分析,说明B在高压下变成液态或固体,由此分析解答。
A.题目中没有给出初始时容器体积,无法计算反应物A的初始浓度,也就无法计算在此条件下用A表示的反应速率,A项错误;
B.由气体状态方程PV=nRT,得P=![]() RT即P=cRT,当温度一定时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,B项错误;
RT即P=cRT,当温度一定时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,B项错误;
C.由B项分析可知压强从2×105Pa增大到5×105Pa时平衡没有移动,说明反应前后气体分子数相等,即m+n=p。再从表格数据看,压强从5×105Pa增大到1×106Pa,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol,浓度增大的倍数大于2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面分析可推断B在此压强下变成了液体或固体,所以压强为1×106Pa时B不是气体,其浓度视为常数,在平衡常数表达式中不应出现,即K=![]() ,C项错误;
,C项错误;
D.其它条件相同时,对于气体参加的反应增大压强反应速率增大,所以压强分别为1×106Pa、5×105Pa、2×105Pa下达到平衡(拐点)时所用时间依次增大。由B项分析知压强从2×105Pa增大到5×105Pa平衡没有移动,A的转化率相同。由C项分析知压强从5×105Pa增大到1×106Pa平衡向逆反应方向移动,A的转化率减小,图像与事实相符,D项正确;答案选D。