题目内容
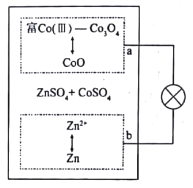
【题目】氨氮废水超标排放是水体富营养化的重要原因,可用以下流程处理:

下列说法正确的是
A.过程I中发生的化学反应属于氧化还原反应
B.过程Ⅱ中![]() ,每转化
,每转化![]() 转移的电子数为6NA
转移的电子数为6NA
C.过程Ⅲ中CH3OH→CO2,甲醇作还原剂
D.过程Ⅲ中HNO3→N2,转移10mol e-时可生成N2 11.2L(标准状况)
【答案】C
【解析】
A.过程I相当于向含![]() 的溶液中加碱加热,将
的溶液中加碱加热,将![]() 转变为氨气,此过程不是氧化还原反应,A项错误;
转变为氨气,此过程不是氧化还原反应,A项错误;
B.![]() 中的氮元素是-3价,
中的氮元素是-3价,![]() 中的氮元素是+5价,因此每转化1mol
中的氮元素是+5价,因此每转化1mol![]() 要转移8mol电子,B项错误;
要转移8mol电子,B项错误;
C.根据氢+1价氧-2价的规则不难看出甲醇中的碳是-2价,而![]() 中的碳是+4价,因此甲醇变成
中的碳是+4价,因此甲醇变成![]() 的过程中甲醇被氧化,作还原剂,C项正确;
的过程中甲醇被氧化,作还原剂,C项正确;
D.硝酸中的氮是+5价的,转化为氮气中0价的氮需要得到5个电子,因此转移10mol电子可以得到2mol的0价氮原子,即1mol氮气,D项错误;
答案选C。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
【题目】下列除杂试剂或操作选用不正确的是( )
物质(括号内为杂质) | 除杂试剂或操作 | |
A | Na2CO3晶体(NaHCO3) | 加热 |
B | CO2(HCl) | 饱和氯化钠溶液、浓H2SO4,洗气 |
C | Fe2O3(SiO2) | NaOH 溶液,过滤 |
D | 稀盐酸(Cl2) | 光照 |
A.AB.BC.CD.D