题目内容
8.写出下列反应的离子方程式(1)试写出少量NaHS04溶液和Ba(HC03)2溶液反应的离子方程式:H++SO42-+Ba2++HCO3-=BaSO4↓+CO2↑+H2O
(2)往FeBr2溶液中,缓缓通入C12充分反应后,经测定有1/3的Br-被氧化,试写出其总反应的离子方程式6Fe2++4Br-+5Cl2═6Fe3++2Br2+10Cl-(已知:还原性Fe2+>Br-)
分析 (1)硫酸氢钠少量,离子方程式按照硫酸氢钠的化学式组成书写,碳酸氢根离子部分反应;
(2)还原性Fe2+>Br-,亚铁离子优先被氧化,溴离子有1/3的被氧化时,亚铁离子已经完全被氧化,根据溴化亚铁的化学式计算出参加反应的亚铁离子和溴离子的物质的量之比,再计算出反应的化学方程式.
解答 解:(1)少量NaHS04溶液和Ba(HC03)2溶液,反应生成碳酸氢钠、硫酸钡沉淀、二氧化碳气体和水,反应的离子方程式为:H++SO42-+Ba2++HCO3-=BaSO4↓+CO2↑+H2O,
故答案为:H++SO42-+Ba2++HCO3-=BaSO4↓+CO2↑+H2O;
(2)亚铁离子的还原性大于溴离子,亚铁离子优先被氧化,有1/3的Br-被氧化,则亚铁离子完全被氧化,参加反应的亚铁离子和溴离子的物质的量之比为:1:(2×$\frac{1}{3}$)=3:2,反应的离子方程式为:6Fe2++4Br-+5Cl2═6Fe3++2Br2+10Cl-,
故答案为:6Fe2++4Br-+5Cl2═6Fe3++2Br2+10Cl-.
点评 本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的书写原则,试题侧重考查反应物过量情况对生成物的影响,有利于培养学生灵活应用基础知识的能力.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
19.某有机物的结构简式为CH2=CHCH2CHO,下列对其化学性质的判断中不正确的是( )
| A. | 能被银氨溶液氧化 | |
| B. | 能使KMnO4酸性溶液褪色 | |
| C. | 1mol该有机物只能与1mol H2发生加成反应 | |
| D. | 1mol该有机物只能与1mol Br2发生加成反应 |
16.下列物质不可以导电的是( )
| A. | 甲苯 | B. | 金属Cu | C. | NaCl溶液 | D. | HCl溶液 |
3.常温时,0.01mol•L-1某一元弱酸的电离常数Ka=10-6,则下列说法正确的是( )
| A. | 上述弱酸溶液的pH=4 | |
| B. | 加入NaOH溶液后,弱酸的电离平衡向右移动,K值增大 | |
| C. | 加入等体积0.01 mol•L-1 NaOH溶液后,所得溶液的pH=7 | |
| D. | 加入等体积0.01 mol•L-1 NaOH溶液后,所得溶液的pH<7 |
17.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,11.2 L的己烷所含的分子数为0.5 NA 个 | |
| B. | 28 g乙烯所含共用电子对数目为6 NA个 | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA个 | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为6 NA个 |
18.下列有机分子中,所有原子不可能处于同一平面内的是( )
| A. | CH2=CH2 | B. | CH2=CH-CH=CH2 | C. | 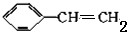 | D. | 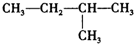 |
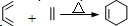
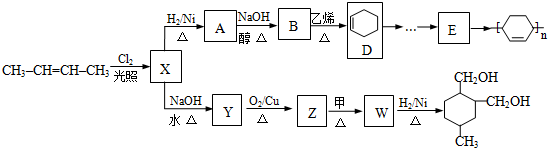
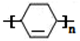
 ;Z→W
;Z→W .
.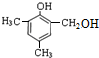 等.
等. ;
;