题目内容
18.下列反应的离子方程式中,正确的是( )| A. | 稀硫酸与氢氧化钡反应:Ba2++SO42-═BaSO4↓ | |
| B. | 铁和稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化铜溶于稀硫酸:Cu(OH)2+2H+═2H2O+Cu2+ | |
| D. | 盐酸与石灰石溶液反应:CO32-+2H+═H2O+CO2↑ |
分析 A.漏写生成水的离子反应;
B.反应生成硫酸亚铁和氢气;
C.反应生成硫酸铜和水;
D.碳酸钙在离子反应中保留化学式.
解答 解:A.稀硫酸与氢氧化钡反应的离子反应为2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O,故A错误;
B.铁和稀盐酸的离子反应为Fe+2H+═Fe2++H2↑,故B错误;
C.氢氧化铜溶于稀硫酸的离子反应为Cu(OH)2+2H+═2H2O+Cu2+,故C正确;
D.盐酸与石灰石溶液反应的离子反应为CaCO3+2H+═H2O+CO2↑+Ca2+,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
8.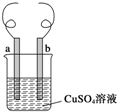 用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
 用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )| A. | 构成原电池时 b 极反应为:Cu-2e-═Cu2+ | |
| B. | 构成电解池时 a 极质量一定减少 | |
| C. | 构成的原电池或电解池工作后都能产生大量气体 | |
| D. | 构成电解池时 b 极质量可能减少也可能增加 |
13.下列反应的离子方程式书写正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 钠与硫酸氢钾溶液反应:2Na+2H+═2Na++H2↑ | |
| C. | 过氧化钠与水反应:2O${\;}_{2}^{2-}$+2H2O═4OH-+O2↑ | |
| D. | 铝粉与NaOH溶液反应:2Al+2OH-+2H2O═2AlO${\;}_{2}^{-}$+H2↑ |
10.蔗糖晶体中滴2~3滴水,再滴入适量的浓硫酸.发现加水处立即变黑,黑色区不断扩大,最后变成一块疏松的焦炭,并伴有刺激性气味气体产生,该实验中浓硫酸表现的性质有( )
①.溶于水放出大量热 ②高沸点难挥发 ③酸性 ④强氧化性 ⑤吸水性 ⑥脱水性.
①.溶于水放出大量热 ②高沸点难挥发 ③酸性 ④强氧化性 ⑤吸水性 ⑥脱水性.
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ①④⑤⑥ | D. | ③④⑤⑥ |
7.下列实验操作中错误的是( )
| A. | 试用分液漏斗分液时,应将漏斗颈上的玻璃塞打开 | |
| B. | 蒸馏实验不一定使用温度计 | |
| C. | 用CCl4萃取碘水中的碘 | |
| D. | 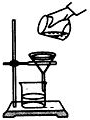 过滤(如图)时,可将悬浊液从烧杯直接倒入漏斗中 过滤(如图)时,可将悬浊液从烧杯直接倒入漏斗中 |
19.为探究Na、Mg、Al的金属活动性顺序,某课外小组同学进行了如下实验:
(1)请在下表中填写与实验步骤对应的实验现象编号:
(2)请写出钠与水反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(3)实验结论金属性强弱顺序是Na>Mg>Al.
(4)请补充该小组同学用原子结构理论解释的上述实验结论:
同周期元素从左至右原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐减小,原子核对电子的引力逐渐增强,失电子能力逐渐减弱,非金属性(填“金属性”或“非金属性”)逐渐减弱.
| 实验步骤 | 1将一小块金属钠放入滴有酚酞溶液的冷水中 2将一小段用砂纸打磨后的镁带,放入试管中,加入少量水,加热至水沸腾,再向试管中滴加酚酞溶液 3将一小段镁带投入稀盐酸中 4将一小片铝投入稀盐酸中. |
| 实验现象 | A剧烈反应,迅速生成大量的气体 B浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红 C反应不剧烈,产生无色气体 D有气体产生,溶液变成红色 |
| 实验步骤 | 1 | 2 | 3 | 4 |
| 实验现象 |
(3)实验结论金属性强弱顺序是Na>Mg>Al.
(4)请补充该小组同学用原子结构理论解释的上述实验结论:
同周期元素从左至右原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐减小,原子核对电子的引力逐渐增强,失电子能力逐渐减弱,非金属性(填“金属性”或“非金属性”)逐渐减弱.
 反应类型:加聚反应
反应类型:加聚反应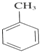 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$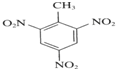 +3H2O.
+3H2O.