题目内容
2.在元素周期表中,在金属与非金属的分界线附近可找到( )| A. | 新型催化剂 | B. | 新型农药 | ||
| C. | 半导体材料 | D. | 耐腐蚀的合金材料 |
分析 元素周期表金属元素与非金属元素的分界线附近的元素,既有金属性也有非金属性,性质决定用途,以此来解答.
解答 解:A.做催化剂的元素从过渡元素区寻找,故A不选;
B.制农药的元素在周期表右上方的非金属元素区寻找,故B不选;
C.作半导体材料的元素,在元素周期表金属元素与非金属元素的分界线附近寻找,故C选;
D.耐高温的合金材料在过渡元素区寻找,故D不选.
故选C.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置及性质为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
17.下列有关原电池的说法正确的是( )
| A. | 原电池中由电能转化为化学能 | B. | 原电池中失电子的电极作负极 | ||
| C. | 原电池的负极发生还原反应 | D. | 原电池中电子由正极流向负极 |
14.7.4g某饱和一元醇X与足量金属Na反应,产生标准状况下H2 1.12L,则饱和一元醇X的可能结构有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
11.红辣椒中含有多种色泽鲜艳的天然色素,其中呈深红色的色素是辣椒红.依据下列结构简式判断,下列说法中正确的是( )
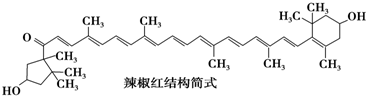

| A. | 不能发生氧化反应 | B. | 属于芳香族化合物 | ||
| C. | 能发生消去反应 | D. | 分子中含有11个碳碳双键 |
12.含有下列离子的溶液中分别加入NaOH固体,能引起该离子浓度减小(溶液体积不变)的是( )
| A. | Cl- | B. | CO32- | C. | HCO3- | D. | AlO2- |

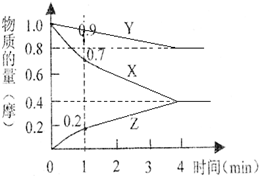 某温度时,2L的密闭容器中X、Y、Z三种物质的物质的量随时间的变化如下图所示.
某温度时,2L的密闭容器中X、Y、Z三种物质的物质的量随时间的变化如下图所示.