题目内容
【题目】设NA为阿伏加德罗常数的值.下列叙述正确的是( )
A.标准状况下,11.2 L SO3所含的氧原子数为1.5NA
B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA
C.常温常压下,7.8 gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8 NA
D.在含Al3+总数为NA的AlCl3溶液中,Cl﹣总数为3NA
【答案】C
【解析】解:A.标况下,三氧化硫不是气体,不能使用气体摩尔体积,故A错误;B.电解精炼铜时,阳极粗铜中含有活泼性较强的铁、锌等杂质,电解时铁、锌杂质先放电,且铁摩尔质量小于铜的64g/mol,锌的摩尔质量大于铜的摩尔质量,所以阳极减少6.4g,转移的电子的物质的量不一定为0.2mol,故B错误;
C.7.8gNa2S和Na2O2的物质的量为: ![]() =0.1mol,过氧化钠中阳离子为过氧根离子,硫化钠中阴离子为硫离子,则0.1mol混合物中含有0.1mol阴离子,含有的阴离子数等于0.1NA , 故C正确;
=0.1mol,过氧化钠中阳离子为过氧根离子,硫化钠中阴离子为硫离子,则0.1mol混合物中含有0.1mol阴离子,含有的阴离子数等于0.1NA , 故C正确;
D.铝离子为弱碱阳离子,水溶液中部分发生水解,在含Al3+总数为NA的AlCl3溶液中,Cl﹣总数大于3NA , 故D错误;
故选:C.

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
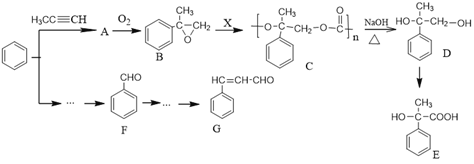
优百分课时互动系列答案【题目】降低太气中CO2含量及有效开发利用CO2 , 是科学家研究的重要课题.
(1)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)△H=122.4kJmol﹣1
①某温度下,将2.0molCO2(g)和6.0molH2(g)充入体积可变的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中.CH3OCH3(g)的物质的量分数变化如下表所示.
P1 | P2 | P3 | |
T1 | 0.10 | 0.04 | 0.02 |
T2 | 0.20 | 0.16 | 0.05 |
T3 | 0.40 | 0.35 | 0.20 |
则P1P3 (填“>”“<”或“=”,下同).若T1、P1 , T3、P3时平衡常数分别为K1、K3 , 则K1K3 . T1、P1时H2的平衡转化率为 .
②一定条件下,上述反应在密闭容器中达平衡.当仅改变影响反应的一个条件,引起的下列变化能说明平衡一定向正反应方向移动的是 .
a.反应物的浓度降低
b.容器内压强增大
c.正反应速率大于逆反应速率
d.化学平衡常数K增大
(2)碳酸氢钾溶液加水稀释, ![]() (填“增大”“不变”或“减小”).用碳酸钾溶液吸收空气中CO2 , 当溶液呈中性时,下列关系或说法正确的是: . a.c(K+)=2c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
(填“增大”“不变”或“减小”).用碳酸钾溶液吸收空气中CO2 , 当溶液呈中性时,下列关系或说法正确的是: . a.c(K+)=2c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
b.c(HCO3﹣)>c(CO32﹣)
c.降低温度,c(H+)c(OH﹣)不变
(3)向盛有FeCl3溶液的试管中滴加少量碳酸钾溶液,立即产生气体,溶液颜色加深,用激光笔照射能产生丁达尔效应,反应的离子方程式为 .
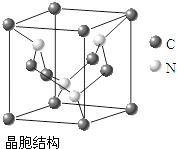
【题目】H、C、N、O、都属于自然界中常见非金属元素.
(1)O、C、N三种元素的第一电离能由小到大顺序是;NH4+中氮原子轨道的杂化类型为 .
(2)CO、N2的结构可表示为:C≡O、N≡N两者的键能数据:(单位kJ/mol)
A﹣B | A=B | A≡B | |
CO | 357.7 | 798.9 | 1071.9 |
N2 | 154.8 | 418.4 | 941.7 |
结合数据说明CO比N2活泼的原因 .
(3)乙二胺(H2N﹣CH2﹣CH2﹣NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 .
(4)C、N元素形成的新材料具有如右图所示结构,该晶体硬度将超过目前世界上最硬的金刚石,成为首屈一指的超硬新材料.该物质的化学式为: .