题目内容
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、常温常压下,28g N2所含有的原子数目为2NA |
| B、42g C2H4和C3H6的混合物中原子数为3NA |
| C、12g金刚石中的C-C键数目为4NA个 |
| D、标准状况下,NA个H2O占有的体积为22.4L |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.28g氮气的物质的量为1mol,1mol氮气中含有2mol氮原子;
B.C2H4和C3H6的最简式为CH2,根据最简式计算出混合物中含有的原子数目;
C.金刚石晶体中,每个C与其它4个C形成了4个C-C共价键,根据均摊法计算出12gC形成的共价键数目;
D.标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算水的体积.
B.C2H4和C3H6的最简式为CH2,根据最简式计算出混合物中含有的原子数目;
C.金刚石晶体中,每个C与其它4个C形成了4个C-C共价键,根据均摊法计算出12gC形成的共价键数目;
D.标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算水的体积.
解答:
解:A.28g氮气的物质的量为1mol,含有2molN原子,所含有的原子数目为2NA,故A正确;
B.42gC2H4和C3H6的混合物中含有3mol最简式CH2,含有9mol原子,混合物中含有的原子数为9NA,故B错误;
C.12g金刚石中含有12gC,含有1molC,金刚石中,每个C与其它4个C形成了4个C-C共价键,每个C形成的共价键数目为:
×4=2,所以1molC形成的共价键为2mol,12g金刚石中的C-C键数目为2NA个,故C错误;
D.标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的体积,故D错误;
故选A.
B.42gC2H4和C3H6的混合物中含有3mol最简式CH2,含有9mol原子,混合物中含有的原子数为9NA,故B错误;
C.12g金刚石中含有12gC,含有1molC,金刚石中,每个C与其它4个C形成了4个C-C共价键,每个C形成的共价键数目为:
| 1 |
| 2 |
D.标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的体积,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为难点、易错点,注意使用均摊法计算金刚石中含有的共价键数目.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某有机物中间体结构如图所示,它不能发生的反应类型是( )
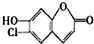

| A、加成反应 | B、取代反应 |
| C、水解反应 | D、消去反应 |
已知下列反应:
Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O
2FeCl3+2KI═2FeCl2+I2+2KCl Cl2+2FeCl2═2FeCl3
则下列物质氧化性由强到弱的顺序是( )
Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O
2FeCl3+2KI═2FeCl2+I2+2KCl Cl2+2FeCl2═2FeCl3
则下列物质氧化性由强到弱的顺序是( )
| A、I2>FeCl3>Cl2>Co2O3 |
| B、Co2O3>Cl2>FeCl3>I2 |
| C、Cl2>Co2O3>I2>FeCl3 |
| D、Cl2>I2>Co2O3>FeCl3 |
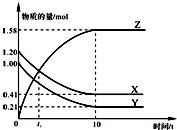 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A、反应开始到10 s,用Z表示的反应速率为0.158 mol/(L?s) |
| B、反应开始到10 s时,Y的转化率为79.0% |
| C、t1时,Z和X的浓度相等,达到了化学平衡状态 |
| D、反应的化学方程式为:X(g)+Y(g)?Z(g) |
在氢氧化钠的溶液中能大量共存且溶液为无色的一组离子是( )
| A、K+、HCO3-、Cl-、SO42- |
| B、S2-、CO32-、CH3COO-、K+ |
| C、K+、Mg2+、SO42-、Na+ |
| D、Na+、MnO4-、NO3-、SO42- |
设NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、1mol CH4(g)和2mol O2(g)的能量总和小于1mol CO2(g)和2mol H2O(g)的能量总和 |
| B、标准状况下,44.8L NO与22.4L O2混合后气体中分子总数小于2NA |
| C、1mol Fe在氧气中充分燃烧失去3NA个电子 |
| D、在标准状况下,NA个CHCl3分子所占的体积约为22.4L |
常温时,下列各组离子在指定溶液中一定不能大量共存的是( )
| A、含有大量NO3-的溶液中:Na+、OH-、I-、SO32- |
| B、pH<7的溶液中:Cu2+、Fe3+、NO3-、Cl- |
| C、使石蕊试液变蓝的溶液中:K+、SO32-、S2-、CO32- |
D、c( )=0.1mol/L的溶液中:Na+、Fe3+、SO42-、NO3- )=0.1mol/L的溶液中:Na+、Fe3+、SO42-、NO3- |
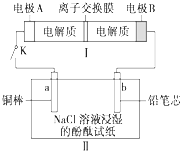 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
| ||
| 放电 |
| A、负极反应为4Na-4e-═4Na+ |
| B、闭合K后,b电极附近的pH变小 |
| C、闭合K后,a电极上有气体产生 |
| D、当有0.01mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112mL |