题目内容
下列关于各图的叙述中,正确的是
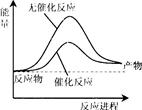
A.图甲表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量
B.图甲表示2 mol H2(g)所具有的能量比2 molH2O(g)所具有的能量多483.6 kJ
C.图乙表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同温、同浓度的NaA溶液的pH小于NaB溶液的pH
D.图乙中起始时HA的物质的量浓度大于HB
C
解析试题分析:A、图甲中反应物的总能量高于生成物的总能量,反应是放热反应,因此表示1mol H2 (g)完全燃烧生成水蒸气放出483.6kJ÷2=241.8 kJ热量,A不正确;B、图甲表示2mol H2(g)和1mol氧气所具有的能量比2molH2O(g)所具有的能量多483.6 kJ,B不正确;C、根据图乙可知,在稀释过程中HA的pH变化程度大于HB的变化程度,所以HA的酸性大于HB的酸性。酸越弱,相应的钠盐越容易水解,所以同温、同浓度的NaA溶液的pH小于NaB溶液的pH,C正确;D、HA的酸性大于HB的酸性,所以图乙中起始时HA的物质的量浓度小于HB,D不正确,答案选C。
考点:考查反应热、弱电解质的电离、盐类水解以及溶液酸碱性的判断等

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案已知:N2(g)+3H2(g) 2NH3(g)△H=" —92" kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
2NH3(g)△H=" —92" kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
| | H2(g) | N2(g) | NH3(g) |
| 1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
B.a的数值为391
C.Q1的数值为92
D.相同条件下,反应物若为2molN2和6molH2,放出热量Q2>2Q1
下列有关化学反应与能量的说法正确的是
| A.酸碱中和是放热反应 |
| B.炭在氧气中燃烧属于吸热反应 |
| C.化学键的形成需吸收能量 |
| D.化学反应过程中,化学能一定转化成热能 |
已知:S(s)+O2(g)→SO2(g) +297.16kJ,2SO2(g)+O2(g) 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是
| A.1 molSO2(g)的能量总和大于lmol S(s)和l molO2(g)的能量总和 |
| B.将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出196.6kJ的热量 |
C.S(g)+O2(g) SO2(g)+Q,Q值小于297.16 kJ SO2(g)+Q,Q值小于297.16 kJ |
| D.当l mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46kJ的热量 |
已知2H2(g)+O2(g)→2H2O(g)+483.6kJ。下列说法或表达正确的是
| A.在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 |
| B.H2(g)+1/2 O2(g)→H2O(1)+Q1;Q1>241.8kJ |
| C.H2(g)+ 1/2O2(g)→H2O(1)+Q2;Q2<241.8kJ |
| D.任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
下列有关能量的判断或表示方法正确的是( )
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
B.从C(石墨) → C(金刚石) Q Q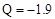 kJ,可知石墨比金刚石更稳定 kJ,可知石墨比金刚石更稳定 |
C.由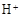 (aq) (aq) (aq) → H2O(l) (aq) → H2O(l) Q Q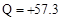 kJ,可知:含1mol CH3COOH的稀溶液与含1mol NaOH的稀溶液混合,放出热量等于57.3 kJ kJ,可知:含1mol CH3COOH的稀溶液与含1mol NaOH的稀溶液混合,放出热量等于57.3 kJ |
D.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g) O2(g) → 2H2O(l) O2(g) → 2H2O(l) Q Q 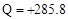 kJ kJ |
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3一kJ/mol、2800 kJ/mol。则下列热化学方程式正确的是
A.C(s)+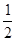 O2(g)=CO(g);△H=" -" 393.5 kJ/mol O2(g)=CO(g);△H=" -" 393.5 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l);△H="+571.6" kJ/mol |
| C.CH4(g)+CO2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol |
D.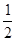 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H="-1400" kJ/mol C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H="-1400" kJ/mol |
已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol,下列叙述正确的是( )
| A.2个氢分子和1个氧分子反应生成2个水分子,放出热量571.6 kJ |
| B.2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),吸收热量571.6 kJ |
| C.2 mol H2O(l)分解为2 mol H2(g)和1 mol O2(g),吸收热量571.6 kJ |
| D.2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),放出热量571.6 kJ |
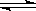 C达到平衡后,无论加压或降温,B的转化率都增大,则下列结论正确的是( )
C达到平衡后,无论加压或降温,B的转化率都增大,则下列结论正确的是( )