��Ŀ����
����Ŀ��
��������������H2O ��H2O2 ��Ba(OH)2 ��Na2O2 ��Cl2 �� Ar ��CO2 ��������ա� ��1��4С������ţ�
��1�� �����Ӽ��ͷǼ��Լ����ɵ���
��2�� �ɼ��Լ��ͷǼ��Լ����ɵ���
��3�� �����ڻ�ѧ������
��4�� ���ۻ�������
��5�� д���������ʵĵ���ʽ��Na2O2
��ijԪ��ԭ�ӵļ۵��ӹ���Ϊ4s24p1�������ڵ�________����________�壬��________��Ԫ��
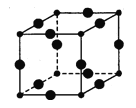
��Cu3N�ľ����ṹ��ͼ��N3-����λ��Ϊ ��Cu+�뾶Ϊacm��N3-�뾶Ϊbcm��Cu3N���ܶ�Ϊ g��cm-3��(�����ӵ�������NA��ʾ,Cu��N��Է�������Ϊ64��14)
���𰸡���1���� ��2���� ��3���� ��4���٢ڢ� ��5��![]() ��.�� ��A p ��.6��103/[4NA(a+b)3]
��.�� ��A p ��.6��103/[4NA(a+b)3]
��������
�����������H2O���ɼ��Լ����ɵļ��Է��ӣ���H2O2�Ǻ��м��Լ��ͷǼ��Լ��ļ��Է��ӣ� ��Ba(OH)2 ���ɱ����Ӻ����������ӹ��ɵ����ӻ�������������Ӻ��м��Թ��ۼ��� ��Na2O2 �ɹ��������Ӻ������ӹ��ɵģ������������к��зǼ��Թ��ۼ�����Cl2 �Ǻ��зǼ����ķǼ��Է��ӣ��� Ar ����ԭ�ӹ��ɵķ��Ӿ��壬�������κλ�ѧ���� ��CO2���зǼ��Լ������ڷǼ��Է��ӡ� ��1�� �����Ӽ��ͷǼ��Լ����ɵ����ܣ���Ϊ���ܣ���2�� �ɼ��Լ��ͷǼ��Լ����ɵ����ڣ���Ϊ���ڣ���3�� �����ڻ�ѧ�������ޣ���Ϊ���ޣ���4�� ���ۻ��������٢ڢߣ���Ϊ���٢ڢߣ���5�� Na2O2���������Ӻ��������ӹ��ɵ����ӻ��������ʽΪ��![]() ����Ϊ��
����Ϊ��![]() ����ijԪ��ԭ�ӵļ۵��ӹ���Ϊ4s24p1�����ݸ�Ԫ�صļ۲�����Ų�ʽ��֪������Ӳ���Ϊ4��λ�ڵ������ڣ��۲������Ϊ3����������p��Ԫ�أ����Ը�Ԫ��λ�ڵ���������A �壬��Ϊ���� ��A p����Cu3N�ľ����ṹ��ͼ��Cu,+λ����ߣ�N3-λ�ڶ��㣬����N3-����Ҿ�����ȵ�Cu+�ĸ���Ϊ6������N3-����λ��Ϊ6���þ�����Cu+�ĸ���Ϊ12��1/4=3��N3-λ�ڶ��㣬����Ϊ8��1/8=1��Cu+�뾶Ϊacm��N3-�뾶Ϊbcm����������Ϊ��2a+2b��cm��Cu3N���ܶ�Ϊ103/[4NA(a+b)3]g��cm-3����Ϊ��6��103/[4NA(a+b)3].
����ijԪ��ԭ�ӵļ۵��ӹ���Ϊ4s24p1�����ݸ�Ԫ�صļ۲�����Ų�ʽ��֪������Ӳ���Ϊ4��λ�ڵ������ڣ��۲������Ϊ3����������p��Ԫ�أ����Ը�Ԫ��λ�ڵ���������A �壬��Ϊ���� ��A p����Cu3N�ľ����ṹ��ͼ��Cu,+λ����ߣ�N3-λ�ڶ��㣬����N3-����Ҿ�����ȵ�Cu+�ĸ���Ϊ6������N3-����λ��Ϊ6���þ�����Cu+�ĸ���Ϊ12��1/4=3��N3-λ�ڶ��㣬����Ϊ8��1/8=1��Cu+�뾶Ϊacm��N3-�뾶Ϊbcm����������Ϊ��2a+2b��cm��Cu3N���ܶ�Ϊ103/[4NA(a+b)3]g��cm-3����Ϊ��6��103/[4NA(a+b)3].