��Ŀ����
����Ŀ�������������������������������й㷺��Ӧ�á�
(1)��ʡ��ؿ�չ�������д����������������������һ����Ҫ�ٴ롣ij�нֵ�����Ͱ��ͼ��ʾ����ش��������⣺

��ͼ�б�ʶ�����ʣ����ڽ������ϵ���__________(д��һ�ּ���)��
��ʹ�����Ͻ�����Ͳ���ŵ���____ (д��һ�㼴��)��ijƷ�����ϵĿ�������Ӧ����_____(�����ɻ������������ɻ�����)Ͳ�С�
������Ʒ��ʴ�Ĺ��̣�ʵ���������������е�________������ѧ��Ӧ�Ĺ��̣���ȥ����Ʒ������������ϡ���ᣬ��Ӧ�Ļ�ѧ����ʽΪ________________________________
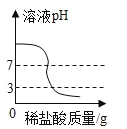
(2)���ס��ҡ������ֽ����ֱ�Ͷ��ϡ�����У��ס������������ݲ������������������������������������Һ�У�һ��ʱ��ı����б��������ɴ��ƶ������ֽ����Ļ����ǿ������˳����________________��
(3)��һ�����������ۼӵ�Al(NO3)3��Cu(NO3)2��AgNO3�������ʵĻ����Һ�У���ַ�Ӧ����ˣ��õ���Һ������������˵����ȷ����________ (����ĸ)��
A.����ҺΪ��ɫ����������һ��������������ͭ
B.����Һ�к�������ͭ����������Һ��һ������Al3����Fe3����NO3��
C.����ҺΪdz��ɫ����������һ��������ͭ����
D.�������м�ϡ���������ݲ���������Һ��һ����Al3����Fe2����Cu2����������Ag��
���𰸡�������Ͳ�������Ͻ���Ͳ ����ʴ��ǿ �ɻ��� ˮ������ Fe2O3+6HCl�T2FeCl3+3H2O ��>��>�� A
��������
�������еĽ��������ʺ���;�Ĺ�ϵ���������˳���Լ����ʼ�ķ�Ӧ���з�����ɡ�
��1���ٽ������ϰ�������������Ͻ�������ͼʾ��ʶ�����������ڽ������ϵ���������Ͳ�������Ͻ���Ͳ���ʴ�Ϊ��������Ͳ�������Ͻ���Ͳ��
������Ʒ����ʴ��ǿ����ʹ�����Ͻ�����Ͳ���ŵ��ǿ���ʴ��ǿ����������Ӧ����ɻ���Ͳ�У��ʴ�Ϊ������ʴ��ǿ���ɻ��գ�
������Ʒ��ʴʵ���������������е�ˮ������������ѧ��Ӧ�Ĺ��̣���ȥ����Ʒ������������ϡ���ᣬ��Ӧ�Ļ�ѧ����ʽΪFe2O3+6HCl�T2FeCl3+3H2O���ʴ�Ϊ��ˮ��������Fe2O3+6HCl�T2FeCl3+3H2O��
��2�����ס��ҡ������ֽ����ֱ�Ͷ��ϡ�����У��ס������������ݲ�����������������˵���ҵĻ���������������������������Һ�У�һ��ʱ��ı����б�������˵���Ļ��ǿ�ڱ������ɴ��ƶ������ֽ����Ļ����ǿ������˳���Ǽ�>��>�ң��ʴ�Ϊ����>��>�ң�
��3����һ�����������ۼ��뵽Al(NO3)3��Cu(NO3)2��AgNO3�������ʵĻ����Һ�У�����������������Ӧ��Ȼ���ٺ�����ͭ��Ӧ��������������Ӧ����ַ�Ӧ����ˣ��õ���Һ��������
A. ����ҺΪ��ɫ����˵���������û��˳�����ͭ���ӿ���û�к�����Ӧ��Ҳ���ܷ�Ӧ��һ���֣���������һ��������������ͭ��A����ȷ��
B. �������к�������ͭ������˵�����ǹ����ģ�������ͭ���û��˳�������������Fe2+������Һ��һ������Al3+��Fe2+��NO3��B�����
C. ����ҺΪdz��ɫ��˵����������Ӧ������Fe2+��������ֻ��AgNO3��Ӧ��Ҳ���ܼȺ�AgNO3��Ӧ��Ҳ��Cu(NO3)2��Ӧ����������һ����������һ������ͭ�����Ậ������C�����
D. �������м�ϡ���������ݲ�����˵����û��ʣ�࣬����Һ��һ����Al3+��Fe2+��������Ag+��Cu2+��D�����
��ѡA��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�