题目内容
【题目】下表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题:

(1)画出A的原子结构示意图________。
(2)A、B、E、F、G五种元素所形成的气态氢化物最稳定的是________(填化学式)。
(3)D在元素周期表中的位置是第3周期________族。
(4)E、F元素的最高价氧化物对应水化物的酸性较强的是: ________(用化学式表示)。
(5)写出C和G形成化合物的电子式________。
【答案】![]() HF ⅢA H2SO4
HF ⅢA H2SO4 ![]()
【解析】
根据元素在周期表中的位置,A、B、C、D、E、F、G分别是O、F、Na、Al、P、S、Cl元素。结合原子结构和元素的性质分析解答。
根据元素在周期表中的位置知,A、B、C、D、E、F、G分别是O、F、Na、Al、P、S、Cl元素。
(1)A为O元素,原子核外有2个电子层、最外层有6个电子,原子结构示意图为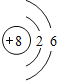 ,故答案为:
,故答案为: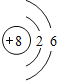 ;
;
(2)同一周期从左到右,元素的非金属性逐渐增强,同一主族从上到下,元素的非金属性逐渐减弱,元素的非金属性越强,其气态氢化物越稳定,这几种元素中非金属性最强的是F元素,则气态氢化物稳定性最强的是HF,故答案为:HF;
(3)D是Al元素,Al原子核外有3个电子层、最外层电子数是3,所以D位于第三周期第ⅢA族,故答案为:ⅢA;
(4)同一周期从左到右,元素的非金属性逐渐增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,E的非金属性小于F,所以E、F元素的最高价氧化物对应水化物的酸性较强的是H2SO4,故答案为:H2SO4;
(5)C是Na元素、G是Cl元素,二者通过得失电子形成离子化合物NaCl,其电子式为![]() ,故答案为:
,故答案为:![]() 。
。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目