题目内容
17.在下列溶液中,各组离子一定能够大量共存的是( )| A. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ | |
| B. | 由水电离的c(H+)=10-12 mol/L的溶液:K+、Ba2+、Cl-、Br- | |
| C. | 在pH=12溶液中:NH4+、K+、NO3-、Cl- | |
| D. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- |
分析 A.使酚酞试液变红的溶液中存在大量氢氧根离子,铁离子与氢氧根离子反应;
B.由水电离的c(H+)=10-12 mol/L的溶液为酸性或碱性溶液,溶液中存在大量的氢离子或氢氧根离子,四种离子之间不反应,都不与氢离子和氢氧根离子反应;
C.在pH=12溶液中存在大量氢氧根离子,铵根离子与氢氧根离子反应;
D.硝酸根离子在酸性溶液中能够氧化亚铁离子、溴离子.
解答 解:A.使酚酞试液变红的溶液为碱性溶液,溶液中存在大量氢氧根离子,Fe3+与氢氧根离子反应生成氢氧化铁沉淀,在溶液中不能大量共存,故A错误;
B.由水电离的c(H+)=10-12 mol/L的溶液中存在大量氢氧根离子或氢离子,K+、Ba2+、Cl-、Br-之间不反应,都不与氢离子和氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.在pH=12溶液为碱性溶液,溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.NO3-在的强酸性溶液中具有强氧化性,能够氧化Fe2+、Br-,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.需要加入适当的氧化剂才能实现的是反应是( )
| A. | 浓HCl→Cl2 | B. | MnO2-→Mn2+ | C. | SO2→HSO3- | D. | Al(OH)3→AlO2- |
5.实验室从海带灰中提取碘的操作过程中,选用的仪器不平确的是( )
| A. | 称取3g左右的干海带-托盘天平 | |
| B. | 过滤煮沸后的海带灰和水的混合物-漏斗 | |
| C. | 灼烧干海带至完全变成灰烬-蒸发皿 | |
| D. | 用四氯化碳从氧化后的海带灰浸取液中提取碘-分液漏斗 |
12.如图为中学化学实验中的常见实验装置
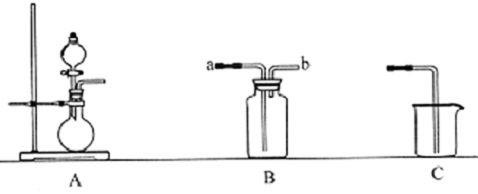
(1)装置A可用于制备多种气体.请写出用A装置制备下列气体时.圆底烧瓶和分液漏斗中应装入的化学试剂.
(2)装置B收集多种气体,若要用于收集氨气.则进气管为b(填字母):
若要收集NO,简述用装置B收集NO的方法将B瓶中装满水,塞上橡皮塞,从b口通入NO气体,将水从a口排出.
(3)现要用上述装置制取Cl2设计实验比较氯元素和硫元索的非金属性的强弱.请在表格内依次填上所需的装置和所发生的离子反应方程式(可不填满).

(1)装置A可用于制备多种气体.请写出用A装置制备下列气体时.圆底烧瓶和分液漏斗中应装入的化学试剂.
| 气体 | O2 | CO2 | NH3 |
| 试剂 |
若要收集NO,简述用装置B收集NO的方法将B瓶中装满水,塞上橡皮塞,从b口通入NO气体,将水从a口排出.
(3)现要用上述装置制取Cl2设计实验比较氯元素和硫元索的非金属性的强弱.请在表格内依次填上所需的装置和所发生的离子反应方程式(可不填满).
| 装置 | 离子方程式 |
2.在密闭容器中发生反应aA(g)?cC(g)+dD(g),反应达到平衡后,将容器体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
| A. | A的转化率变大 | B. | 平衡向逆反应方向移动 | ||
| C. | C的体积分数变大 | D. | a>c+d |
6.核原料${\;}_{92}^{235}$U裂变释放出${\;}_{55}^{131}$I和${\;}_{55}^{137}$Cs,关于它们的说法正确的是( )
| A. | ${\;}_{92}^{235}$U和${\;}_{53}^{131}$I是同位素 | |
| B. | ${\;}_{53}^{131}$I的质子数为131 | |
| C. | ${\;}_{92}^{235}$U的中子数是143 | |
| D. | ${\;}_{53}^{131}$I和${\;}_{55}^{137}$Cs是同种元素 |
7.互称为同分异构体的物质不可能是( )
| A. | 同系物 | B. | 具有相同的分子式 | ||
| C. | 具有相同的通式 | D. | 具有相同的相对分子质量 |
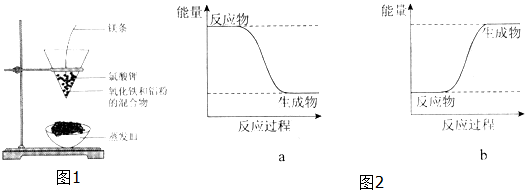
 Al2O3+2 Fe,其能量变化可用图2中的a(填“a”或“b”)表示.
Al2O3+2 Fe,其能量变化可用图2中的a(填“a”或“b”)表示.