题目内容
如图为反应2X(g)+Y(s)  2Z(g)的反应过程和能量关系图,下列说法正确的是( )
2Z(g)的反应过程和能量关系图,下列说法正确的是( )
| A.曲线a和b表示两个反应过程的反应热不同 |
| B.曲线a一定表示反应是在无催化剂时的反应过程 |
| C.增大压强,X的转化率一定增大 |
| D.反应达到平衡后,升高温度,平衡常数K值一定减小 |
D
解析试题分析:由盖斯定律知,反应热由始态和终态决定,a和b的初始态和终态一样,故反应热相同;影响反应过程的因素很多,有温度、压强、催化剂等,B中曲线a与b可能使用不同的催化剂所致。
考点:考查基本理论,化学反应平衡

 名校课堂系列答案
名校课堂系列答案下列说法正确的组合是( )
(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应
(2)物质发生化学变化都伴有能量的变化
(3)伴有能量变化的物质变化都是化学变化
(4)吸热反应和放热反应都有可能自发进行
(5)Na转化为Na+时,吸收的能量就是该过程的反应热
(6)水蒸气变为液态水时放出的能量就是该变化的反应热
| A.(1)(2) | B.(3)(5) | C.(2)(6) | D.(2)(4) |
已知反应:
①101 kPa时,2C(s)+O2(g) =2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq) =H2O(l) ΔH=-57.3 kJ·mol-1
③在同温同压下,S(g)+O2(g)=SO2(g) ΔH1
下列结论正确的是( )
| A.H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol |
| B.C的标准燃烧热为-110.5 kJ·mol-1 |
| C.稀醋酸与稀NaOH溶液反应生成1 mol水放出的热量为57.3 kJ |
| D.由③知S(s)+O2(g)=SO2(g)ΔH2则ΔH2>ΔH1 |
已知下列反应的热化学方程式
6C(s)+5H2(g)+3N2(g)+9O2(g) 2C3H5(ONO2)3(l) ΔH1
2 H2(g)+ O2(g) 2H2O(g) ΔH2
C(s)+ O2(g) CO2(g) ΔH3
则反应4C3H5(ONO2)3(l) 12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为
| A.12ΔH3+5ΔH2-2ΔH1 | B.2ΔH1-5ΔH2-12ΔH3 |
| C.12ΔH3-5ΔH2-2ΔH1 | D.ΔH1-5ΔH2-12ΔH3 |
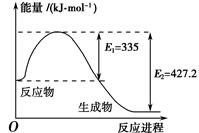
已知:
| A.-393.5kJ/mol | B.-679.3 kJ/mol | C.-787 k J/mol | D.+180.9 kJ/mol |
为了测定酸碱中和反应的中和热,计算时至少需要的数据是
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量
⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
| A.①②③⑥ | B.①③④⑥ | C.③④⑤⑥ | D.全部 |
下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的△H=2×283.0kJ/mol |
如图为某烯烃在催化剂作用下发生加成反应的能量变化图,下列有关叙述错误的是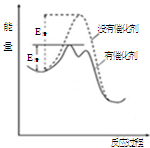
| A.催化剂能降低该反应的活化能 |
| B.催化剂能改变该反应的焓变 |
| C.该反应为放热反应 |
| D.由图可知,在催化剂作用下,该反应不是一步完成的 |
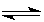 2NH3(g) ΔH=a kJ·mol-1。
2NH3(g) ΔH=a kJ·mol-1。