题目内容
【题目】ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用图1所示装置模拟工业制取并收集ClO2。
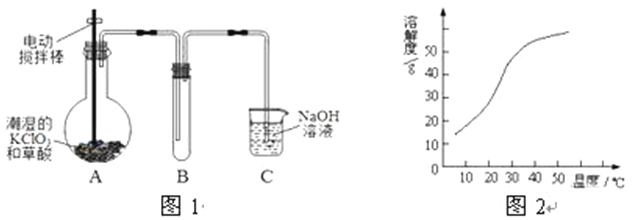
(1) A 装胃电动搅抖柞的作用是___________
(2)B装置必须放在冰水浴中,其原因是___________
(3)反应后在装置C中可得NaClO2溶液。已知I.NaClO2饱和溶液在温度低了38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2, 温度高于60℃时NaClO2分解生成NaClO3和NaCl;
Ⅱ.NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①减压,55℃蒸发结晶;②__________;③用38℃~60℃热水洗涤;④_____;得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL(已知2 Na2S2O3+ I2=Na2S4O6+ 2NaI)。
①配制100 mLcmol·L-1Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:____________。
②原ClO2溶液的浓度为_________g/L(用含字母代数式表示)。
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____________。(填“偏高”、“偏低”或“不变” )
【答案】 增大反应物的接触面积,加快反应速率 使ClO2充分冷凝,减少挥发 趁热过滤 低于60℃干燥 100mL容量瓶、胶头滴管 135cV2/V1 偏高
【解析】(1)A装置电动搅拌棒的作用是反应时搅拌,增大反应物的接触面积,加快反应速率;(2)B装置必须放在冰水浴中,其原因是使ClO2充分冷凝,减少挥发;(3)①减压,55℃蒸发结晶;②趁热过滤;③用38℃~60℃热水洗涤;④低于60℃干燥;得到成品。(4)①配制100 mL c mol/LNa2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有100 mL的容量瓶、胶头滴管;②设原ClO2溶液的物质的量浓度为x,根据反应2ClO2+10I-+8H+= 5I2+2Cl-+4H2O、2Na2S2O3+ I2=Na2S4O6+ 2NaI,则关系:
2ClO2~~~~~~~~~~~~~~5I2~~~~~~~~~~~~~~~10Na2S2O3
2 10
x×V1mL×10-3L/mL×![]() cmol·L-1×V2mL×10-3L/mL
cmol·L-1×V2mL×10-3L/mL
x=![]() mol/L,故原ClO2溶液的浓度为
mol/L,故原ClO2溶液的浓度为![]() g/L;③若滴定前滴定管尖嘴中有气泡,则滴定前读数偏小,而滴定后气泡消失,则消耗的标准溶液体积偏大,所以测定结果就偏高。
g/L;③若滴定前滴定管尖嘴中有气泡,则滴定前读数偏小,而滴定后气泡消失,则消耗的标准溶液体积偏大,所以测定结果就偏高。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案