题目内容
1.(某无色溶液,由Na+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种组成.取适量该溶液进行如下实验:①加入过量盐酸,有气体生成;
②在上面所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
③在②所得溶液中再加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出.
(1)则原溶液中一定不能大量存在的离子是Ba2+、Al3+、Fe3+,可能存在的离子是SO42-.
(2)实验①中发生反应的离子方程式为AlO2-+4H+=Al3++2H2O,CO32-+2H+=H2O+CO2↑.
(3)实验②中气体成分是CO2 ,沉淀甲的成分是Al(OH)3.
(4)实验③中气体成分是NH3,沉淀乙的成分是BaCO3或BaCO3与BaSO4的混合物.
分析 (1)碳酸根和盐酸反应产生二氧化碳气体,钡离子、铝离子、三价铁离子和碳酸根不共存,碳酸氢铵溶液和盐酸反应产生二氧化碳气体,HCO3-和AlO2-反应产生氢氧化铝沉淀,Ba(OH)2溶液和碳酸氢铵溶液反应产生氨气和碳酸钡白色沉淀;
(2)实验①中偏铝酸根离子和酸反应生成铝离子,碳酸根离子和氢离子反应生成二氧化碳和水;
(3)过量盐酸中加入过量碳酸氢铵溶液,碳酸氢铵溶液和盐酸反应产生二氧化碳气体;碳酸氢铵溶液中的HCO3-和AlO2-之间能反应产生氢氧化铝沉淀;
(4)②所得溶液中有剩余的碳酸氢铵,Ba(OH)2溶液能和碳酸氢铵溶液反应产生氨气和碳酸钡白色沉淀,硫酸根是否存在不确定,可能有BaSO4.
解答 解:(1)所有离子中只有碳酸根和盐酸反应产生气体二氧化碳,所以一定含有碳酸根离子,而钡离子、铝离子、三价铁离子和碳酸根不共存,所以一定没有钡离子、铝离子、三价铁离子,溶液中必须有阳离子,所以一定含有钠离子,过量盐酸中加入过量碳酸氢铵溶液,碳酸氢铵溶液和盐酸反应产生二氧化碳气体,碳酸氢铵溶液中的HCO3-和AlO2-之间能反应产生氢氧化铝沉淀,所以一定含有AlO2-,②所得溶液中有剩余的碳酸氢铵,Ba(OH)2溶液能和碳酸氢铵溶液反应产生氨气和碳酸钡白色沉淀,所以硫酸根是否存在不确定,
故答案为:Ba2+、Al3+、Fe3+;SO42-;
(2)①加入过量盐酸,有气体生成,只有碳酸根和盐酸反应产生气体二氧化碳,CO32-+2H+=H2O+CO2↑,根据以上分析还有H+和AlO2-之间反应,AlO2-+4H+=Al3++2H2O,
故答案为:AlO2-+4H+=Al3++2H2O;CO32-+2H+=H2O+CO2↑;
(3)②在上面所得的溶液中再加入过量碳酸氢铵溶液,过量盐酸中加入过量碳酸氢铵溶液,碳酸氢铵溶液和盐酸反应产生二氧化碳气体,碳酸氢铵溶液中的HCO3-和AlO2-之间反应产生氢氧化铝沉淀,
故答案为:CO2;Al(OH)3;
(4)铵根离子和氢氧根离子反应生成氨气,碱性溶液中碳酸氢根离子和碱反应生成碳酸根离子,碳酸根离子和钡离子反应生成碳酸钡沉淀,硫酸根是否存在不确定,可能有BaSO4,
故答案为:NH3;BaCO3或BaCO3与BaSO4的混合物.
点评 本题考查了常见离子的检验方法,题目难度中等,注意根据溶液呈电中性判断溶液中存在的离子方法,本题充分考查了学生的分析、理解能力,要求熟练掌握常见离子的检验方法.

| A. | 热稳定性:H2O>HF>H2S | |
| B. | NH4Cl的电子式: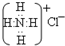 | |
| C. | 反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | |
| D. | 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
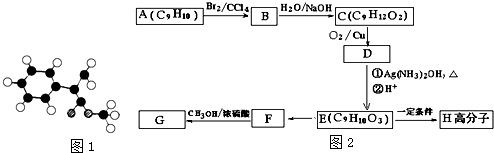
 ;
;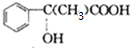 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$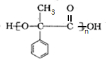 +(n-1)H2O.
+(n-1)H2O.