题目内容
6.A、B、C、D、E、F为六种20号以前的元素,其核电荷数依次增大,A、B同周期,两者相隔一元素;B、D同主族相邻,A、B、D三种元素的核电荷数之为和30.已知A是形成化合物种类最多的元素,C、E能形成CE型化合物.已知E的单质为黄绿色气体,F的次外层有8个电子,已知它的最外不止一个电子.回答:(1)写出各元素名称:碳、氧、钠、硫、氯
(2)A、D、E最高价氧化物的水化物酸性由强到弱的顺序:(用化学式填空,下同)HClO4>H2SO4>H2CO3
(3)比较A、B气态氧化物的稳定性:CH4<H2O
(4)比较D、E氢化物的还原性:H2S>HCl.
分析 A、B、C、D、E、F为六种20号以前的元素,其核电荷数依次增大,设B的原子序数为x,因A、B同周期,两者相隔一元素,且原子序数A<B,所以A的原子序数为x-2,B、D同主族相邻,则D的原子序数为x+8,因A、B、D三种元素的核电荷数之为和30,则有 x+x-2+x+8=30,解得x=8,即B为O元素,A为C元素,D为S元素;F的次外层有8个电子,已知它的最外层不止一个电子,且原子序数大于S,所以F为Ca元素;E介于D与F之间,E的单质为黄绿色气体,且能形成化合物CE,所以E为Cl元素,C为Na元素,由此分析解答.
解答 解:A、B、C、D、E、F为六种20号以前的元素,其核电荷数依次增大,设B的原子序数为x,因A、B同周期,两者相隔一元素,且原子序数A<B,所以A的原子序数为x-2,B、D同主族相邻,则D的原子序数为x+8,因A、B、D三种元素的核电荷数之为和30,则有 x+x-2+x+8=30,解得x=8,即B为O元素,A为C元素,D为S元素;F的次外层有8个电子,已知它的最外层不止一个电子,且原子序数大于S,所以F为Ca元素;E介于D与F之间,E的单质为黄绿色气体,且能形成化合物CE,所以E为Cl元素,C为Na元素,
(1)A、B、C、D、E为六种元素的符号分别为 C、O、Na、S、Cl,则名称为碳、氧、钠、硫、氯,故答案为:碳、氧、钠、硫、氯;
(2)A、D、E最高价氧化物的水化物分别为:H2CO3、H2SO4、HClO4,根据非金属性越强,对应元素最高价氧化物的水化物的酸性越强可知,非金属性Cl>S>C,所以酸性由强到弱的顺序为:HClO4>H2SO4>H2CO3,故答案为:HClO4>H2SO4>H2CO3;
(3)根据非金属性越强,氢化物越稳定可知,O的非金属性大于C,所以氢化物的稳定性CH4<H2O,故答案为:CH4<H2O;
(4)非金属性越强,离子的还原性越弱,Cl的非金属性大于S所以还原性H2S>HCl,故答案为:H2S>HCl.
点评 本题考查原子结构与元素周期律,元素的推断是解答的关键.利用元素周期表元素位置关系列式求出元素的原子序数是此题的难点.

 阅读快车系列答案
阅读快车系列答案| A. | 盐酸 | B. | 二氧化碳 | C. | 硝酸 | D. | 乙醇 |
| A. | 水 | B. | 食盐 | C. | 纯碱 | D. | 酒精 |
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点:H2T<H2R | B. | M与T形成的化合物具有两性 | ||
| C. | 单质与稀盐酸反应的速率:L<Q | D. | L2+与R2-的核外电子数相等 |
| A. | 新制氯水--棕色瓶、阴凉处 | B. | 氢氟酸--橡皮塞、玻璃瓶 | ||
| C. | 少量金属钠--广口瓶、煤油里 | D. | 稀盐酸--细口瓶、阴凉处 |
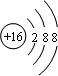 ;A与C组成的化合物电子式为
;A与C组成的化合物电子式为 .
.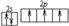
 ,C离子的电子排布式为1s22s22p63s23p6
,C离子的电子排布式为1s22s22p63s23p6