题目内容
8.设NA是阿伏伽德罗常数的数值,下列说法正确的是( )| A. | 1molAl3+离子含有的电子数为3NA | |
| B. | 1molCl2含有1 NA个原子 | |
| C. | 23g钠在22.4L(标况下)Cl2中反应,转移电子数NA个 | |
| D. | 欲配制1.00L 1.00mol.L-1的NaCl溶液,可将 58.5gNaCl溶于 1.00L水中 |
分析 A、铝离子含有10个电子;
B、氯气为双原子分子;
C、23g钠的物质的量为1mol,标况下22.4L氯气的物质的量为1mol,反应时氯气过量;
D、将58.5g氯化钠溶于1L水中,溶液体积大于1L.
解答 解:A、铝离子含有10个电子,故1mol铝离子中含10mol电子即10NA 个,故A错误;
B、氯气为双原子分子,故1mol氯气中含2mol氯原子即2NA个,故B错误;
C、23g钠的物质的量为1mol,标况下22.4L氯气的物质的量为1mol,反应时氯气过量,钠完全反应,由于反应后变为+1价,故1mol钠转移1mol电子即NA个,故C正确;
D、将58.5g氯化钠溶于1L水中,溶液体积大于1L,则所得溶液的浓度小于1mol/L,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18. 已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
(1)写出碳酸的第一步电离平衡常数表达式:Ka1=$\frac{c({H}^{+})•c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}$.
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:H2CO3>HSO3->HCO3-.
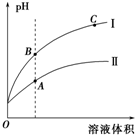
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化图象中,曲线I表示的酸是CH3COOH(填化学式).
②a、b、c三点中,水的电离程度最大的是C(填字母).
 已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:| 醋酸 | 碳酸 | 亚硫酸 |
| Ka=1.75×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:H2CO3>HSO3->HCO3-.
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化图象中,曲线I表示的酸是CH3COOH(填化学式).
②a、b、c三点中,水的电离程度最大的是C(填字母).
19.下列物质的转化过程须加氧化剂的是( )
| A. | CuO→Cu | B. | MnO4-→Mn2+ | C. | Na2SO3→Na2SO4 | D. | Cl2→Cl- |
3.在硫化氢的水溶液中,存在以下平衡:H2S═HS-H+、HS-═H++S2-,若使溶液的pH减小,则c(S2-)( )
| A. | 增大 | B. | 减小 | ||
| C. | 不变 | D. | 可能增大也可能减小 |
13.对于CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3kJ•mol-1的叙述正确的是( )
| A. | 该反应是吸热反应 | |
| B. | 反应的△H与各物质的状态有关,与化学计量数也有关 | |
| C. | 由方程式可知,CH4的燃烧热为802.3 kJ•mol-1 | |
| D. | 该式的含义为:25℃、101 kPa下,1molCH4气体完全燃烧生成CO2和液态水时放出热量802.3kJ |
20.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为原来的60%,则( )
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率增大了 | ||
| C. | 物质B的质量分数减小了 | D. | a>b |
18.下列关于钢铁腐蚀的叙述正确的是( )
| A. | 钢铁插入水中,水下部分比空气与水交界处更容易腐蚀 | |
| B. | 钢铁在海水中比在河水中更易腐蚀,主要是由于海水中有大量电解质 | |
| C. | 钢铁设备上连接铜块可以防止钢铁腐蚀 | |
| D. | 钢铁设备与外加直流电源的正极相连可以防止钢铁腐蚀 |
 ═2KCl+2MnCl2+5Cl2↑+8H2O
═2KCl+2MnCl2+5Cl2↑+8H2O