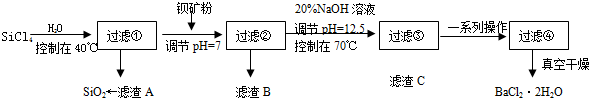
��Ŀ����
2����Է�������Ϊ92�ķ�����X��ú��һ�ָ�����������XΪԭ�Ϻϳ�һϵ�л�����Ʒ����ϳ�·������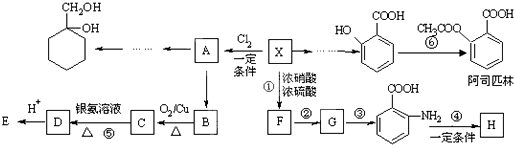
����A��һ�ȴ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO��
��֪��
��
 ��
��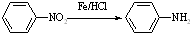 ���������ױ�������
���������ױ��������������ѧ֪ʶ�뱾��������Ϣ�ش��������⣺
��1��G�к��еĹ��������Ȼ��������������ƣ���
��2��H�Ľṹ��ʽ��
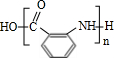 ��
����3����Ӧ��-��������������Ӧ���Тڢݣ�
��4��E�����ں˴Ź�������ʱ����4���壬E��һ��ͬ���칹��K���ܷ���������Ӧ���ܷ���ˮ�ⷴӦ��K������������Һ�з���ˮ��Ļ�ѧ����ʽΪ��
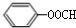 +2NaOH��
+2NaOH��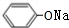 +HCOONa+H2O��
+HCOONa+H2O����5��
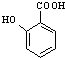 �ж���ͬ���칹�壬���к��������������Ĺ���2�֣�
�ж���ͬ���칹�壬���к��������������Ĺ���2�֣����ܷ���������Ӧ������ˮ��
��ÿĦ��ͬ���칹���������2mol NaOH
�۱�����һ�ȴ���ֻ�����֣�
��6����������ͼ����ʽд����A�Ʊ�
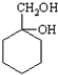 �Ĺ��̣�
�Ĺ��̣�
���� ��Է�������Ϊ92��ij������X����������ΪCxHy����$\frac{92}{12}$=7��8����������Cԭ����Hԭ�ӹ�ϵ��֪��������Cԭ����Ŀ����С��7���ʸ÷�����X�ķ���ʽΪC7H8���ṹ��ʽΪ ��X����������ȡ����Ӧ����A��Aת������B��B����������C��C����������Һ��Ӧ����D����B���д��ǻ���C����ȩ������AΪ
��X����������ȡ����Ӧ����A��Aת������B��B����������C��C����������Һ��Ӧ����D����B���д��ǻ���C����ȩ������AΪ ��BΪ
��BΪ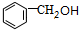 ��CΪ
��CΪ ��D�ữ����E����DΪ
��D�ữ����E����DΪ ��EΪ
��EΪ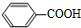 ��
�� ��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ����F����Ϸ�Ӧ�۵IJ����֪FΪ
��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ����F����Ϸ�Ӧ�۵IJ����֪FΪ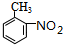 ��Fת������G�����ڱ������ױ��������ɷ�Ӧ��Ϣ��Ӧ��Ϣ���֪��GΪ
��Fת������G�����ڱ������ױ��������ɷ�Ӧ��Ϣ��Ӧ��Ϣ���֪��GΪ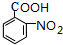 ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO����
��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO���� �ķ���ʽ��ȼ���1����H2O��Ϊ
�ķ���ʽ��ȼ���1����H2O��Ϊ ͨ���γ��ļ��������۷�Ӧ���ɵĸ߾��HΪ
ͨ���γ��ļ��������۷�Ӧ���ɵĸ߾��HΪ ���ɷ�Ӧ��������Ľṹ��֪����Ӧ����
���ɷ�Ӧ��������Ľṹ��֪����Ӧ����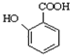 �����ᷢ��ȡ����Ӧ����
�����ᷢ��ȡ����Ӧ����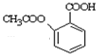 ��
��
��6�� �ڴ��������·����ӳɷ�Ӧ����
�ڴ��������·����ӳɷ�Ӧ����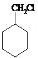 �������������ƴ���Һ�����������·�����ȥ��Ӧ����
�������������ƴ���Һ�����������·�����ȥ��Ӧ���� �������������ӳɷ�Ӧ����
�������������ӳɷ�Ӧ����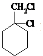 ���������������ˮ��Һ�з���ˮ�ⷴӦ����
���������������ˮ��Һ�з���ˮ�ⷴӦ����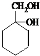 ��
��
��� �⣺��Է�������Ϊ92��ij������X��һ����Ҫ���л�����ԭ�ϣ���������ΪCxHy����$\frac{92}{12}$=7��8����������Cԭ����Hԭ�ӹ�ϵ��֪��������Cԭ����Ŀ����С��7���ʸ÷�����X�ķ���ʽΪC7H8���ṹ��ʽΪ ��X����������ȡ����Ӧ����A��Aת������B��B����������C��C����������Һ��Ӧ����D����B���д��ǻ���C����ȩ������AΪ
��X����������ȡ����Ӧ����A��Aת������B��B����������C��C����������Һ��Ӧ����D����B���д��ǻ���C����ȩ������AΪ ��BΪ
��BΪ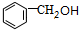 ��CΪ
��CΪ ��D�ữ����E����DΪ
��D�ữ����E����DΪ ��EΪ
��EΪ ��
�� ��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ����F����Ϸ�Ӧ�۵IJ����֪FΪ
��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ����F����Ϸ�Ӧ�۵IJ����֪FΪ ��Fת������G�����ڱ������ױ��������ɷ�Ӧ��Ϣ��Ӧ��Ϣ���֪��GΪ
��Fת������G�����ڱ������ױ��������ɷ�Ӧ��Ϣ��Ӧ��Ϣ���֪��GΪ ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO����
��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO���� �ķ���ʽ��ȼ���1����H2O��Ϊ
�ķ���ʽ��ȼ���1����H2O��Ϊ ͨ���γ��ļ��������۷�Ӧ���ɵĸ߾��HΪ
ͨ���γ��ļ��������۷�Ӧ���ɵĸ߾��HΪ ���ɷ�Ӧ��������Ľṹ��֪����Ӧ����
���ɷ�Ӧ��������Ľṹ��֪����Ӧ���� �����ᷢ��ȡ����Ӧ����
�����ᷢ��ȡ����Ӧ���� ��
��
��1��GΪ �������Ȼ����������ʴ�Ϊ���Ȼ���������
�������Ȼ����������ʴ�Ϊ���Ȼ���������
��2��������������֪��H�Ľṹ��ʽ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3����Ӧ��-���У���Ӧ�٢�����ȡ����Ӧ����Ӧ�ڢ�����������Ӧ����Ӧ�����ڻ�ԭ��Ӧ����Ӧ���������۷�Ӧ���ʴ�Ϊ���ڢݣ�
��4��EΪ �������ں˴Ź�������ʱ����4���壬E��һ��ͬ���칹��K���ܷ���������Ӧ���ܷ���ˮ�ⷴӦ��KΪ
�������ں˴Ź�������ʱ����4���壬E��һ��ͬ���칹��K���ܷ���������Ӧ���ܷ���ˮ�ⷴӦ��KΪ ��������������Һ�з���ˮ��Ļ�ѧ����ʽΪ��
��������������Һ�з���ˮ��Ļ�ѧ����ʽΪ�� +2NaOH��
+2NaOH�� +HCOONa+H2O��
+HCOONa+H2O��
�ʴ�Ϊ��4�� +2NaOH��
+2NaOH�� +HCOONa+H2O��
+HCOONa+H2O��
��5��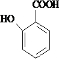 �ж���ͬ���칹�壬���з��Ϣ��ܷ���������Ӧ������ˮ�⣬����-CHO��û����������ÿĦ��ͬ���칹���������2mol NaOH������2�����ǻ����۱�����һ�ȴ���ֻ�����֣����������Ŵ��ڼ�λ����λ��ȩ�������м䣬�ʷ���������ͬ���칹�干��2�֣�
�ж���ͬ���칹�壬���з��Ϣ��ܷ���������Ӧ������ˮ�⣬����-CHO��û����������ÿĦ��ͬ���칹���������2mol NaOH������2�����ǻ����۱�����һ�ȴ���ֻ�����֣����������Ŵ��ڼ�λ����λ��ȩ�������м䣬�ʷ���������ͬ���칹�干��2�֣�
�ʴ�Ϊ��2��
��6�� �ڴ��������·����ӳɷ�Ӧ����
�ڴ��������·����ӳɷ�Ӧ���� �������������ƴ���Һ�����������·�����ȥ��Ӧ����
�������������ƴ���Һ�����������·�����ȥ��Ӧ���� �������������ӳɷ�Ӧ����
�������������ӳɷ�Ӧ���� ���������������ˮ��Һ�з���ˮ�ⷴӦ����
���������������ˮ��Һ�з���ˮ�ⷴӦ���� ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ��Ѷ��еȣ�����X����Է��������ƶ�X�Ľṹ�ǽ���Ĺؼ������A�ķ�Ӧ����Ľṹ�ص㣬�ж�A�Ľṹ���ٸ��ݷ�Ӧ��������Ӧ��Ϣ�������Ʒ������Ʒ����Ͻ����жϣ��Ƕ��л���֪ʶ���ۺϿ��飬�ܽϺõĿ���ѧ�����Ķ���������˼ά���������л��ȵ����ͣ�

| A�� | ��һ����Ԫ�� | B�� | ��${\;}_{26}^{56}$Fe��Ϊͬ�������� | ||
| C�� | ��һ����ԭ�� | D�� | ��������Ϊ26 |
| A�� | ������ | B�� | 1��2-������ | C�� | 1��3-������ | D�� | �Ҷ��� |
�ٱ���Na2CO3��Һ
��Na2SiO3��Һ
��NaAlO2��Һ
��Ca��ClO��2��Һ
��CaCl2��Һ��
| A�� | �ڢ� | B�� | �ڢۢ� | C�� | �٢ڢ� | D�� | ȫ�� |
| A�� | 25��ʱ��pH=13��1.0L Ba��OH��2��Һ�к��е�Ba2+��ĿΪ0.05NA | |
| B�� | ��״���£�2.24L CH2Cl2ֻ���е�C-Cl������ĿΪ0.2NA | |
| C�� | 1.8g��ˮ��D2O��ֻ����NA������ | |
| D�� | ���³�ѹ�£�21g��ϩ�뻷����Ļ�����к���ԭ����ĿΪ3NA |