题目内容
【题目】t℃时,AgCl(s)与AgI(s)分别在溶液中达到沉淀溶解平衡,相关离子浓度的关系如下图所示。下列说法正确的是

A. 曲线Y表示![]() 与
与![]() 的变化关系
的变化关系
B. t℃时,向Z点对应的溶液中加入蒸馏水,可使溶液变为曲线X对应的饱和溶液
C. t℃时,AgCl(s)+I-(aq)![]() AgI(s)+Cl-(aq)的平衡常数K=1×103
AgI(s)+Cl-(aq)的平衡常数K=1×103
D. t℃时,向浓度均为0.1mol/ L的KI与KCl混合溶液中加入AgNO3溶液,当Cl-刚好完全沉淀时,此时c(I-) = 1×10-11 mol/L
【答案】D
【解析】A. ![]() =16时
=16时![]() ,Ksp=
,Ksp=![]() ,
, ![]() =10时
=10时![]() ,Ksp=
,Ksp=![]() ,由于碘化银的溶度积小于氯化银,故曲线Y表示
,由于碘化银的溶度积小于氯化银,故曲线Y表示![]() 与
与![]() 的变化关系,选项A错误;B. t℃时,向Z点对应的溶液中加入蒸馏水,银离子浓度及卤离子浓度均减小,
的变化关系,选项A错误;B. t℃时,向Z点对应的溶液中加入蒸馏水,银离子浓度及卤离子浓度均减小, ![]() 与
与![]() 均增大,可使溶液变为曲线Y对应的饱和溶液,选项B错误;C、t℃时,AgCl(s)+I-(aq)
均增大,可使溶液变为曲线Y对应的饱和溶液,选项B错误;C、t℃时,AgCl(s)+I-(aq)![]() AgI(s)+Cl-(aq)的平衡常数K=
AgI(s)+Cl-(aq)的平衡常数K=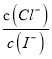 =
=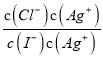 =
=![]() =1×106,选项C错误;D、t℃时,向浓度均为0.1mol/ L的KI与KCl混合溶液中加入AgNO3溶液,当Cl-刚好完全沉淀时,c(Cl-) = 1×10-5 mol/L,c(Ag+) =
=1×106,选项C错误;D、t℃时,向浓度均为0.1mol/ L的KI与KCl混合溶液中加入AgNO3溶液,当Cl-刚好完全沉淀时,c(Cl-) = 1×10-5 mol/L,c(Ag+) = ![]() =1×10-5 mol/L,此时c(I-) =
=1×10-5 mol/L,此时c(I-) = ![]() =1×10-11 mol/L,选项D正确。答案选D。
=1×10-11 mol/L,选项D正确。答案选D。

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目