��Ŀ����
����Ŀ�����̷��з��ֵĻ���ԭ�������谷���������з�Ӧ�ϳɣ�CaO��3C![]() CaC2��CO����CaC2��N2
CaC2��CO����CaC2��N2![]() CaCN2��C��CaCN2��2H2O=NH2CN��Ca(OH)2��NH2CN��ˮ��Ӧ��������[CO(NH2)2]�����غϳ������谷��
CaCN2��C��CaCN2��2H2O=NH2CN��Ca(OH)2��NH2CN��ˮ��Ӧ��������[CO(NH2)2]�����غϳ������谷��
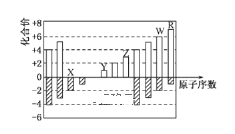
(1)��̬��ԭ�ӵ���ռ�ݵ�����ܲ������_________��������______�ֲ�ͬ�����ĵ��ӡ�
(2)CaCN2��������ΪCN22-����CN22-��Ϊ�ȵ�����ķ�����N2O���ɴ˿�����֪CN22-�Ŀռ乹��Ϊ________��
(3)1mol���ط���[CO(NH2)2]�к��е���������������Ŀ֮��Ϊ_________������Ԫ�صĵ縺���ɴ�С��˳��Ϊ_____________��
(4)�����谷�׳�������������ṹΪ��
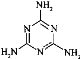
���е�ԭ�ӵ��ӻ���ʽΪ________��
���𰸡�N 6 ֱ���� 1:7 O>N>C>H sp2 sp3
��������
(1)�Ƶ�ԭ������Ϊ20����̬��ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p64s2��
(1)�Ƶ�ԭ������Ϊ20����̬��ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p64s2������ռ�ݵ�����ܲ������N���Ӳ㣬�ܲ���ͬ��ͬһ�ܼ��ϵĵ��ӣ����ӵ���չ����ͬ����������ͬ����ͬ�����ĵ�����Ŀ���ܼ���Ŀ��ȣ�������6�ֲ�ͬ�����ĵ��ӣ��ʴ�Ϊ��N��6��
��2��CN22-���ӵ�ԭ�Ӹ���Ϊ3���۵�����Ϊ16����CN22-������ͬԭ�Ӹ����ͼ۵������ĵȵ�����ķ�����N2O��CO2���ȵ����������ͬ�Ŀռ乹�ͣ�CO2�Ŀռ乹��Ϊֱ���Σ���CN22-�Ŀռ乹��Ϊֱ���Σ��ʴ�Ϊ��ֱ���Σ�
��3�����ط�������6��������1��˫����һ����������һ���Ҽ���˫������һ���Ҽ������������������������Ŀ֮��Ϊ1��7��Ԫ�طǽ�����Խǿ���縺��Խ������������Ԫ�صĵ縺���ɴ�С��˳��ΪO>N>C>H���ʴ�Ϊ��1:7��O>N>C>H��
��4�������谷�л��ϵĵ�ԭ����̼ԭ�Ӽ��γ�˫������ԭ�Ӳ���sp2�ӻ��������ϵ�ԭ����̼ԭ�Ӻ���ԭ���Ե�����������ԭ�Ӳ���sp3�ӻ����ʴ�Ϊ��sp2��sp3��