题目内容
【题目】硫单质及其化合物在化工生成等领域应用广泛。
(1)工业尾气中的SO2一直是环境污染的主要原因之一,工业上常采用如下方法降低尾气中的含硫量:
①方法1:燃煤中加入生石灰,将SO2转化为CaSO3,再氧化为CaSO4
已知:a. CaO(s)+CO(g) =CaCO3(s) ΔH=-178.3kJ·mol-1
b.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g) ΔH=-2762.2kJ·mol-1
c.2CaSO3(s)+O2(g)=2CaSO4(s) ΔH=-2314.8kJ·mol-1
写出CaO(s)与SO2(g)反应生成CaSO3(s)的热化学方程式:_________________________________。
②方法2:用氨水将SO2转化为NH4HSO3,再氧化为( NH4)2SO4。
实验测得NH4HSO3溶液中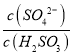 = 1500,则溶液的pH为______________(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)。
= 1500,则溶液的pH为______________(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)。
(2)煤制得的化工原料气中含有羰基硫(0=C=S),该物质可转化为H2S,反应为COS(g) +H2(g)![]() H2S (g)+CO(g) ΔH>0。
H2S (g)+CO(g) ΔH>0。
①恒温恒容条件下,密闭容器中发生上述反应,下列事实不能说明反应达到平衡状态的是__________
(填字母)。
a.COS的浓度保持不变 b.化学平衡常数不再改变
c.混合气体的密度不再改变 d.形成2molH-S键的同时形成1mol H-H键
②T1℃时,在恒容的密闭容器中,将定量的CO和H2S混合加热并达到下列平衡:H2S(g)+ CO(s) ![]() COS(g)+H2(g),K=0 25,则该温度下反应COS(g)+H2(g)=H2S(g)+ CO(s)的平衡常数K=__________。
COS(g)+H2(g),K=0 25,则该温度下反应COS(g)+H2(g)=H2S(g)+ CO(s)的平衡常数K=__________。
T1℃时,向容积为10 L的恒容密闭容器中充入1mol COS(g)和1molH2(g),达到平衡时COS的转化率为______________________。
(3)过二硫酸(H2S2O8)是一种强氧化性酸,其结构式为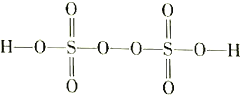 。
。
①在Ag+催化作用下,S2O82-能与Mn2+在水溶液中发生反应生成SO42-和MnO4-,1mol S2O82-能氧化的Mn2+的物质的量为_________mol。
②工业上可用惰性电极电解硫酸和硫酸铵混合溶液制备过二硫酸铵。则阳极的电极反应式为______________________。
【答案】 CaO(s)+SO2(g)==CaSO3(s) ΔH=-402.0kJ·mol-1 6 bc 4 66.7% 0.4 2SO42--2e-=S2O82-
【解析】(1)①(b-c)/2+a CaO(s)+SO2(g)==CaSO3(s) ΔH=-402.0kJ·mol-1
CaO(s)与SO2(g)反应生成CaSO3(s)的热化学方程式:CaO(s)+SO2(g)==CaSO3(s) ΔH=-402.0kJ·mol-1。
②Ka1=(C(H+).C(HSO3-))/C(H2SO3) Ka2=( C(H+). C(SO32-)/ C(HSO3- Ka1Ka2= C2(H+).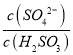 =1.5×10-2×1.0×10-7 C(H+)=1×10-6 溶液的pH为6。
=1.5×10-2×1.0×10-7 C(H+)=1×10-6 溶液的pH为6。
(2)COS(g) +H2(g)![]() H2S (g)+CO(g) ΔH>0。①恒温恒容条件下,密闭容器中发生上述反应,a.COS的浓度保持不变 说明化学反应达到平衡状态了; b.化学平衡常数只和温度有关,不受浓度影响,所以不能作为判断平衡的依据; c.混合气体的密度=m/V, 恒容V定值,都是气体所以m不变。故c不能;d.形成2molH-S键的同时形成1mol H-H键说明正逆反应速率相等,故可以作为判断平衡的标志。答案:b c。
H2S (g)+CO(g) ΔH>0。①恒温恒容条件下,密闭容器中发生上述反应,a.COS的浓度保持不变 说明化学反应达到平衡状态了; b.化学平衡常数只和温度有关,不受浓度影响,所以不能作为判断平衡的依据; c.混合气体的密度=m/V, 恒容V定值,都是气体所以m不变。故c不能;d.形成2molH-S键的同时形成1mol H-H键说明正逆反应速率相等,故可以作为判断平衡的标志。答案:b c。
②T1℃时H2S(g)+ CO(s) ![]() COS(g)+H2(g)K=(C(COS).C(H2))/C(H2S)= 0 25
COS(g)+H2(g)K=(C(COS).C(H2))/C(H2S)= 0 25
,COS(g)+H2(g)=H2S(g)+ CO(s) K= C(H2S)/ (C(COS).C(H2))=1/0 25=4
T1℃时,COS(g) + H2(g) = H2S(g)+ CO(s)
初始量 0.1 0.1 0 0
变化量 X X X X
平衡量 0.1-X 0.1-X X X
(3)K=X/(0.1-X)2=4 X=0.0667 COS的转化率为0.0667/0.1×100%= 66.7% ,答案:66.7%
① 5S2O82-+ 2Mn2+ +8H2O= 10SO42-+2MnO4-+16H+,
5mol 2mol
1mol X X=0.4mol
②用惰性电极电解硫酸和硫酸铵混合溶液制备过二硫酸铵。根据氧化还原原理知SO42-失电子做阳极,阳极的电极反应式为2SO42--2e-=S2O82-。

【题目】由下列实验及现象推出的相应结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 2 mL0.01mol·L-1的KI溶液中滴入等体积等浓度的FeCl3溶液,将充分反应后的溶液分三份,一份滴入K3[Fe(CN)6]溶液,第二份滴入KSCN溶液,第三份滴入淀粉溶液 | 滴入K3[Fe(CN)6]溶液后产生蓝色沉淀;滴入KSCN溶夜后变血红色;滴入淀粉溶液后溶液变蓝 | KI溶液和FeCl3溶液发生反应:2Fe3++2I- |
B | 向稀硫酸中加入铜片,然后通入氧气加热 | 先无明显现象,通入氧气加热后溶液变蓝 | 氧化性:稀硫酸>Cu2+ |
C | 向浓度均为0.1 mol·L-1的Na2SO3和Na2SiO3溶液中分别滴加酚酞 | Na2SiO3溶液红色更深 | 非金属性:Si<S |
D | 将几滴等浓度的FeCl3溶液、AlCl3溶液同时滴入足量等浓度的NaOH溶液中 | 只产生红褐色沉淀 | Ksp[Al(OH)3]>K sp[Fe(OH)3] |
A. A B. B C. C D. D




