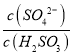题目内容
【题目】加热HCOONa固体,发生的反应有:2HCOONa ![]() Na2C2O4+H2↑ ①
Na2C2O4+H2↑ ①
2HCOONa ![]() Na2CO3 +H2↑+CO↑ ②
Na2CO3 +H2↑+CO↑ ②
Na2C2O4 ![]() Na2CO3 + CO ↑ ③
Na2CO3 + CO ↑ ③
HCOONa加热分解时,固体失重率与温度的关系如右图所示。下列说法正确的是( )

A. T<415℃时,只有反应①发生
B. 反应①、②不可能同时发生
C. 570℃<T<600℃时,残留固体的主要成分是Na2CO3
D. 残留固体中m(Na2C2O4)=m( Na2CO3)时,反应①、②的反应速率相等
【答案】C
【解析】试题分析:A.加热完全分解得到Na2C2O4时,失重率为![]() ×100%≈1.47%<5%,则T<415℃时反应①、②同时发生,A错误;B.由A中分析可知,反应①、②可能同时发生,B错误;C.加热分解完全残留固体为Na2CO3,失重率为
×100%≈1.47%<5%,则T<415℃时反应①、②同时发生,A错误;B.由A中分析可知,反应①、②可能同时发生,B错误;C.加热分解完全残留固体为Na2CO3,失重率为![]() ×100%≈22.1%,则570℃<T<600℃时,残留固体的主要成分是Na2CO3,C正确;D.残留固体中的m(Na2C2O4)=m(Na2CO3)时,无法判断所需时间,不能判断反应①、②的反应速率,D错误,答案选C。
×100%≈22.1%,则570℃<T<600℃时,残留固体的主要成分是Na2CO3,C正确;D.残留固体中的m(Na2C2O4)=m(Na2CO3)时,无法判断所需时间,不能判断反应①、②的反应速率,D错误,答案选C。

练习册系列答案
相关题目