题目内容
8.在一定温度下(SO3为气体),10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达平衡时O2的浓度为0.30mol/L.请计算(写出计算过程):(1)10min内SO3的化学反应速率;
(2)容器内反应前与平衡时的压强之比(最简整数比);
(3)平衡常数K.
分析 在一定温度下(SO3为气体),10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达平衡时O2的浓度为0.30mol/L,则:
2SO2(g)+O2(g)?2SO3(g)
起始量(mol/L):0.5 0.45 0
变化量(mol/L):0.3 0.15 0.3
平衡量(mol/L):0.2 0.3 0.3
(1)根据v=$\frac{△c}{△t}$计算v(SO3);
(2)压强之比等于气体物质的量之比;
(3)平衡常数K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})×c({O}_{2})}$.
解答 解:在一定温度下(SO3为气体),10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达平衡时O2的浓度为0.30mol/L,则:
2SO2(g)+O2(g)?2SO3(g)
起始量(mol/L):0.5 0.45 0
变化量(mol/L):0.3 0.15 0.3
平衡量(mol/L):0.2 0.3 0.3
(1)v(SO3)=$\frac{0.3mol/L}{10min}$=0.03mol/(L.min),
答:10min内SO3的化学反应速率为0.03mol/(L.min);
(2)压强之比等于气体物质的量之比,则容器内反应前与平衡时的压强之比为(5+4.5)mol:(0.2+0.3+0.3)mol/L×10L=19:16,
答:容器内反应前与平衡时的压强之比为19:16;
(3)平衡常数K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})×c({O}_{2})}$=$\frac{0.{3}^{2}}{0.{2}^{2}×0.3}$=7.5,
答:该温度下2SO2(g)+O2(g)?2SO3(g)的平衡常数为7.5.
点评 本题考查化学平衡计算、反应速率计算、平衡常数计算,比较基础,有利于基础知识的巩固.

| A. | 标准状况下,2.24LCH4含有的H原子数为0.1NA | |
| B. | 常温常压下,NA个CO2分子占有的体积为22.4L | |
| C. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3NA | |
| D. | 2.4g金属镁变为镁离子时失去的电子数为0.2 NA |
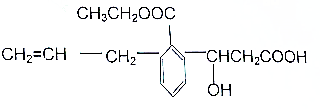
| A. | 可发生的反应类型有:取代、加成、消去、酯化、水解、氧化、中和、聚合 | |
| B. | 1mol该物质与足量NaOH溶液反应,消耗NaOH的物质的量为2mol | |
| C. | 1mol该物质与Na、Na2CO3、NaHCO3反应时,所消耗的物质的量之比为2:1:2,产生的气体在标准状况下的体积比是2:1:2 | |
| D. | 该有机物属于芳香族化合物 |
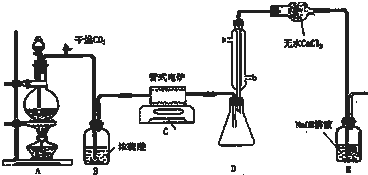
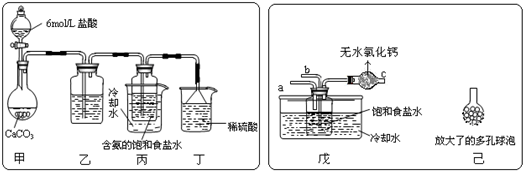
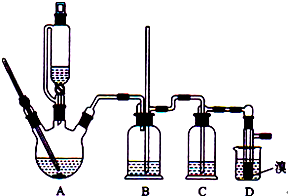 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的副反应有:乙醇在浓硫酸的存在下l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷,装置如图所示:有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能快地把反应温度升高到170℃左右,其目的有ad(填正确选项前的字母)
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”)
(3)实验过程中装置B可以防止倒吸,并检查装置C、D是否堵塞,写出装置D堵塞时B中的现象当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
| A. | X的值为1 | |
| B. | M的平均反应速率为0.15 mol•L-1•min-1 | |
| C. | M的转化率为60% | |
| D. | 平衡时P的浓度为0.25 mol•L-1 |
| A. | 10gH2 | B. | 16gCH4 | C. | 20gSO3 | D. | 17gNH3 |