题目内容
(双项)在标准状况下,将2.24L NH3与4.48L HCl气体充入密闭容器内混合.已知:NH3+HCl═NH4Cl.下列说法正确的是( )
| A、反应中有0.5NA个共价键断裂 |
| B、反应中有0.1NA个离子键形成 |
| C、混合后,容器内物质含有0.5 NA个化学键 |
| D、混合前气体中含有0.5NA个共价键 |
考点:化学键
专题:化学键与晶体结构
分析:根据反应NH3+HCl═NH4Cl中,断裂3个氮氢键、1个氢氯键,同时生成1个离子键,结合各物质的物质的量来解答.
解答:
解:在标准状况下,2.24L NH3与4.48L HCl气体的物质的量分别为0.1mol,0.2mol,由反应NH3+HCl═NH4Cl可知,氯化氢过量,反应中断裂3个氮氢键、1个氢氯键,同时生成1个离子键,氯化铵中含有1个离子键,4个共价键;
A.反应中有0.4NA个共价键断裂,故A错误;
B.反应中有0.1NA个离子键形成,故B正确;
C.混合后,容器内氯化铵中含有0.5 NA个化学键,氯化氢中含有0.1 NA个化学键,故C错误;
D.混合前2.24L NH3与4.48L HCl气体中含有的共价键分别为0.3NA,0.2NA,共含0.5NA个共价键,故D正确;
故选BD.
A.反应中有0.4NA个共价键断裂,故A错误;
B.反应中有0.1NA个离子键形成,故B正确;
C.混合后,容器内氯化铵中含有0.5 NA个化学键,氯化氢中含有0.1 NA个化学键,故C错误;
D.混合前2.24L NH3与4.48L HCl气体中含有的共价键分别为0.3NA,0.2NA,共含0.5NA个共价键,故D正确;
故选BD.
点评:本题主要考查了化学反应中化学键的计算,难度不大,注意反应过程的分析.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案
相关题目
根据酸碱质子理论判定下列说法不正确的是( )
| A、所有的弱酸根都是碱 |
| B、酸式弱酸根既是酸又是碱 |
| C、不可能一种物质既是酸又是碱 |
| D、氢氧根是碱 |
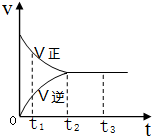 如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( )| A、t1时,只有正方向反应 |
| B、t2时,反应到达限度 |
| C、t2-t3,反应不再发生 |
| D、t2-t3,各物质的浓度不再发生变化 |
下列说法正确的是( )
| A、不含其他杂质的天然油脂属于纯净物 |
| B、油脂在酸性或碱性条件下都比在纯水中易水解 |
| C、各种油脂水解后的产物中都有甘油 |
| D、油脂的烃基部分饱和程度越大,熔点越低 |
一定条件下,可逆反应达到平衡时( )
| A、各组分的浓度不再变化 |
| B、正逆反应速率均为零 |
| C、反应物浓度小于生成物的浓度 |
| D、反应停止了 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1mol Fe在过量的Cl2中充分燃烧,转移的电子数为0.3NA |
| B、常温下,22.4L甲烷中含有的共价键数目为4NA |
| C、2mol SO2和1mol O2在密闭容器中催化加热,充分反应后,容器内分子总数为2NA |
| D、由CO2和O2组成的混合气体中共有NA个分子,其中的氧原子数为2NA |
元素周期表中,划分周期的依据是( )
| A、元素的核电荷数 |
| B、元素原子的电子层数 |
| C、元素的化合价 |
| D、元素原子的最外层电子数 |
下列叙述正确的是( )
| A、加入铝粉能产生H2的溶液中可能大量共存的离子组:NH4+、Fe2+、SO42-、NO3- |
| B、碳酸氢钠溶液中离子浓度的大小关系c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) |
| C、碳酸钠溶液中离子浓度的关系2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、向Ca(ClO)2溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- |
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
| A、加热 |
| B、用98%的浓硫酸代替稀硫酸 |
| C、滴加少量硫酸铜溶液 |
| D、不用铁片改用铁粉 |