题目内容
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
| A、加热 |
| B、用98%的浓硫酸代替稀硫酸 |
| C、滴加少量硫酸铜溶液 |
| D、不用铁片改用铁粉 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:影响铁与稀硫酸反应的因素有浓度、温度、固体表面积大小以及原电池反应等,一般来说,增大浓度、升高温度、增大固体表面积或形成原电池反应都可增大反应速率.
解答:
解:A.加热,温度升高,活化分子的百分数增大,反应速率增大,故A不选;
B.改用98%的浓硫酸,不生成氢气,则生成氢气的反应速率减小,故B选;
C.加少量硫酸铜,锌置换出铜,形成原电池反应,反应速率增大,故C不选;
D.不用铁片,改用铁粉,增大接触面积,反应速率加快,故D不选.
故选B.
B.改用98%的浓硫酸,不生成氢气,则生成氢气的反应速率减小,故B选;
C.加少量硫酸铜,锌置换出铜,形成原电池反应,反应速率增大,故C不选;
D.不用铁片,改用铁粉,增大接触面积,反应速率加快,故D不选.
故选B.
点评:本题考查化学反应速率的影响,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意把握影响化学反应速率的影响和影响原因,难度不大,注意相关基础知识的积累.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
(双项)在标准状况下,将2.24L NH3与4.48L HCl气体充入密闭容器内混合.已知:NH3+HCl═NH4Cl.下列说法正确的是( )
| A、反应中有0.5NA个共价键断裂 |
| B、反应中有0.1NA个离子键形成 |
| C、混合后,容器内物质含有0.5 NA个化学键 |
| D、混合前气体中含有0.5NA个共价键 |
X、Y、Z、W、M为原子序数依次增大的短周期主族元素.已知:①元素对应的原子半径大小为:X<Z<Y<M<W;②Y是组成有机物的必要元素 ③Z与X可形成两种常见的共价化台物,与W可形成两种常见的离子化台物;④M的电子层数与最外层电子数相等.下列说法不正确的是( )
| A、Z、W、M形成的简单离子,其半径大小关系为Z>W>M |
| B、M的最高价氧化物对应的水化物与Y、W两元素最高价氧化物对应的水化物均能反应 |
| C、工业上可用电解熔融的W的氯化物的方法制取W单质 |
| D、Y、Z元素形成的简单氢化物的稳定性:Z>Y |
下列化学用语表达正确的是( )
| A、乙酸的结构简式:CH3-COOH |
B、丙烷分子的比例模型: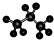 |
C、Ar原子的结构示意图: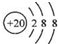 |
D、过氧化氢的电子式: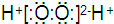 |
X、Y分别是两种药物,其结构如图.
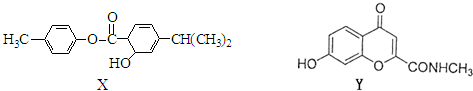
下列说法不正确的是( )
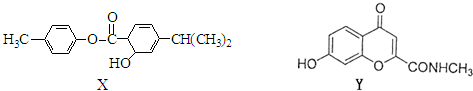
下列说法不正确的是( )
| A、1mol X与NaOH溶液反应,最多消耗2 mol NaOH |
| B、X、Y都有较强的水溶性 |
| C、X、Y都能使KMnO4溶液褪色 |
| D、X、Y的水解产物有可能发生聚合反应 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、澄清透明的溶液中:Na+、K+、MnO4-、AlO2- | ||
| B、0.1mol?L-1 FeCl3溶液:K+、NH4+、I-、SCN- | ||
C、
| ||
| D、c(S2-)=0.1mol?L-1的溶液中:Na+、NH4+、ClO-、SO42- |
化学与生活是紧密相连的,下列说法正确的是( )
| A、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| B、海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化 |
| C、生铁在潮湿的空气中易生锈,其负极反应式为:2H2O+O2+4e-=4OH- |
| D、BaSO4在医学上用做钡餐,Ba2+对人体无毒 |