题目内容
【题目】下表是氧化镁和氯化镁的熔、沸点数据:
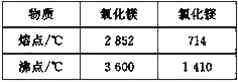
请参考以上数据分析,从海水中提取镁,正确的方法是( )
A.海水![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B.海水![]() MgCl2溶液→MgCl2晶体
MgCl2溶液→MgCl2晶体![]() Mg
Mg
C.海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D.海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液
MgCl2溶液![]() MgCl2(熔融)
MgCl2(熔融)![]() Mg
Mg
【答案】D
【解析】
A.在实际生产中从海水提取MgCl2,用石灰乳而不用NaOH,另外电解氢氧化镁不能得到金属镁,应该电解熔融的氯化镁,故A错误;
B.海水中存在的是氯化镁,加入盐酸不能富集浓缩得到氯化镁溶液,故B错误;
C.过程中氧化镁熔点高,电解消耗大量的能量,应该电解熔融的氯化镁制备镁,故C错误;
D.海水中含有镁离子,向海水中加入石灰乳,将镁离子转化为Mg(OH)2沉淀,反应方程式为:Mg2++2OH-=Mg(OH)2↓,再将Mg(OH)2溶于稀盐酸得到MgCl2溶液,反应为Mg(OH)2+2HCl=MgCl2+2H2O,氯化镁易水解生成氢氧化镁,为防止水解,将MgCl2溶液在HCl氛围中蒸发得到MgCl2,氯化镁熔点较低、氧化镁熔点较高,为降低成本,电解熔融MgCl2得到金属Mg,故D正确;
故选D。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】X、Y、Z、W四种物质间的转化关系如图所示 ,下列转化不能一步实现的是
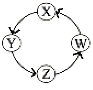
序号 | X | Y | Z | W |
A | N2 | NH3 | NO | NO2 |
B | Na | NaOH | Na2CO3 | NaCl |
C | Cl2 | Ca(ClO)2 | HClO | HCl |
D | H2S | S | SO3 | H2SO4 |
A.AB.BC.CD.D
【题目】某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其它不溶于酸、碱的杂质。部分金属氢氧化物Ksp近似值如下表所示:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
现用含镍废催化剂制备NiSO4·7H2O晶体,其流程图如下:
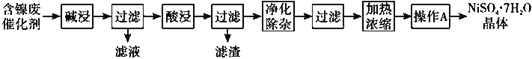
回答下列问题:
(1)“碱浸”时发生反应的离子方程式为2A1+2OH-+2H2O=2AlO2—+3H2↑,_________。
(2)“酸浸”所使用的酸为_____________。
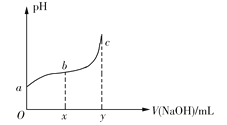
(3)“净化除杂”需加入H2O2溶液,其作用是__________________________。然后调节pH使溶液中铁元素恰好完全沉淀,此时的pH为____________(保留1位小数)。
(4)“操作A”为_____、过滤、洗涤、干燥,即得产品。
(5)NiSO4在NaOH溶液中可被NaClO氧化为NiOOH,该反应的化学方程式为_______。
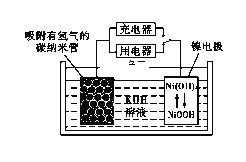
(6)NiOOH可作为镍氢电池的电极材料,该电池的工作原理如下图所示,其充电时,正极的电极反应式为____________。