题目内容
【题目】在元素周期表中,元素的金属性和非金属性及其强弱比较与周期序数(n)和主族序数(A)有如下经验公式:K= ![]() (K为A与n的比值).下列推理正确的是( )
(K为A与n的比值).下列推理正确的是( )
A.当A一定时,K值越小,则元素的非金属性越强
B.当K=0,则该元素系同一周期中最活泼的金属元素
C.当n一定时,随着K值增大,则元素的非金属性逐渐增强
D.当K=l时,则该元素系过渡元素
【答案】C
【解析】解:元素的金属性和非金属性及其强弱比较与周期数(n)和主族数(A)有如下经验公式:K= ![]() (K为A与n的比值).
(K为A与n的比值).
A.当A一定时,K值越小,则周期数n越大,则元素的金属性越强,非金属性越弱,故A错误;
B.当K=0,A为0,为0族元素,即该元素为稀有气体元素,则该元素系同一周期中最不活泼的非金属元素,故B错误;
C.当n一定时,K值越大,则主族数A越大,则元素的非金属性越强,所以随着K值增大,则元素的非金属性逐渐增强,故C正确;
D.当K=l时,周期数=族序数,如Be、Al等,则该元素为两性元素;当K<1时,则周期数大于主族序数,如Na、Mg等,即该元素为金属元素,故D错误;
故选C.

【题目】某研究性学习小组得到一块软锰矿样品,其主要成分为二氧化锰(MnO2)和石英(SiO2)。为了制取氯气并进行氯气的性质实验,其装置如图所示,请回答下列问题:
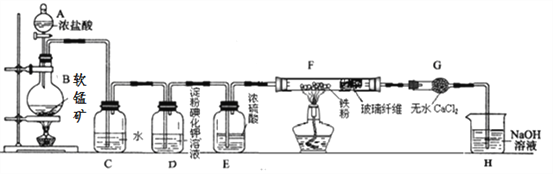
(1)取适量软锰矿置于烧瓶中,加入足量浓盐酸并加热,烧瓶中发生的化学反应为:MnO2 +4HCl(浓)![]() MnCl2+Cl2↑+2H2O。充分反应后烧瓶中残留的固体是____________;若有4mol浓盐酸参与反应,产生的氯气在标准状况下的体积为____22.4L (填“等于”、“小于”或“大于”),浓盐酸在该反应中表现出来的性质_______________________;
MnCl2+Cl2↑+2H2O。充分反应后烧瓶中残留的固体是____________;若有4mol浓盐酸参与反应,产生的氯气在标准状况下的体积为____22.4L (填“等于”、“小于”或“大于”),浓盐酸在该反应中表现出来的性质_______________________;
(2)若将干燥的有色布条放入C中,观察到的现象是 ______ ,原因是 ______________ (用化学方程式和文字回答);
(3)实验中观察到D溶液变蓝色,写出D装置中发生反应的离子方程式 ____________ ;
(4)为探究氯气与Fe反应的产物与氯气通入量的关系,设计实验,并记录现象如下:
实验方法 | 实验现象 | 实验结论 |
1.取反应初始阶段(氯气不足量)F中产物,用磁铁除去过量的Fe,剩余产物溶于水中,取上层溶液装入两只试管中,①加入KSCN溶液,②加入KMnO4溶液 | ①KSCN溶液显红色 ②KMnO4溶液不褪色 | (不填) |
2.取充分反应后(氯气通入足够长时间)F中产物,溶于水中,加入KMnO4溶液 | KMnO4溶液不褪色 |
根据实验现象,得出实验结论,写出氯气与Fe粉共热时发生反应的化学方程式______;
(5)已知F中的产物易潮解,在F和H装置之间安装G装置,目的是_________________。