题目内容
【题目】实验室回收废水中苯酚的过程如图所示。下列分析错误的是( )
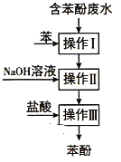
A. 操作Ⅰ中苯作萃取剂,多次萃取后检验是否萃取干净可选择三氯化铁溶液
B. 苯酚钠是离子化合物,在苯中的溶解度比在水中的小
C. 通过操作Ⅱ苯可循环使用, 三步操作均需要分液漏斗,
D. 操作中苯酚碰到皮肤,需用NaOH溶液清洗后,再用大量水不断冲洗
【答案】D
【解析】
用苯萃取废水中的苯酚,进行分液得到苯酚的苯溶液,再加入氢氧化钠溶液,苯酚与氢氧化钠反应得到苯酚钠,苯与苯酚钠溶液不互溶,再进行分液操作,得到苯与苯酚钠溶液,苯可以循环利用,苯酚钠溶液中加入盐酸得到苯酚,经过分液操作进行分离得到苯酚。
用苯萃取废水中的苯酚,进行分液得到苯酚的苯溶液,再加入氢氧化钠溶液,苯酚与氢氧化钠反应得到苯酚钠,苯与苯酚钠溶液不互溶,再进行分液操作,得到苯与苯酚钠溶液,苯可以循环利用,苯酚钠溶液中加入盐酸得到苯酚和NaCl溶液,同样经过分液操作进行分离得到苯酚;
A.操作I是用苯萃取废水中的苯酚,进行分液得到苯酚的苯溶液,苯为萃取剂,检验萃取后的废水中苯酚是否存在可滴加FeCl3溶液,不显紫色,即说明萃取干净,故A正确;
B.苯酚钠属于钠盐,易溶于水,在苯中的溶解度比在水中的小,故B正确;
C.操作Ⅱ得到苯与苯酚钠溶液,苯可以循环利用;操作Ⅰ、Ⅱ、Ⅲ均为分液操作,都用到了分液漏斗,故C正确;
D.氢氧化钠有强腐蚀性,应用酒精溶液清洗,故D错误;
故答案为D。

【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
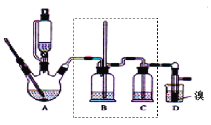
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是____;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置A中除了浓硫酸和乙醇外,还应加入___,其目的是_____,装置A中生成副产物乙醚的化学反应方程式 ______。
(3)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放_____
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液 d.品红和酸性KMnO4
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_____的方法除去。
【题目】I.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
第二周期 | ① | ② | ③ | |||||
第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:________(填元素符号),
(2)在最高价氧化物对应的水化物中,碱性最强的化合物是________(填化学式),在常温下该化合物和元素⑦的单质反应的离子方程式__________。
(3)用电子式表示元素④与⑥的化合物的形成过程:__________。
(4)表示①与⑦的化合物的电子式_______,该化合物是由______(填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是____________(用化学式表示)。
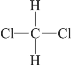
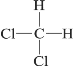
II.①CBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He
只含有离子键的是(用序号回答)_____,即含离子键又含共价键是(用序号回答)_____,其中含有非极性共价键的共价化合物是(用序号回答)_____,常温时为固体,当其熔化时,不破坏化学键的是(用序号回答)_____。