题目内容
16.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )| 选项 | 叙述I | 叙述II |
| A | 苯甲酸的溶解度随温度升高而增大 | 用蒸发浓缩、冷却结晶、过滤,除去苯甲酸中混有的泥沙 |
| B | NH4Cl受热容易分解 | 加热NH4Cl制备NH3 |
| C | SO2具有漂白性 | SO2能使KMnO4溶液褪色 |
| D | 某温度下,碳酸的K1=4.4×10-7,次氯酸的K=2.98×10-8 | 用CO2和NaClO制备HClO |
| A. | A | B. | B | C. | C | D. | D |
分析 A、蒸发结晶析出苯甲酸晶体,过滤不能得到纯净的苯甲酸,应趁热过滤;
B、氯化铵受热易分解,但分解生成的氯化氢和氨气会重新反应生成氯化铵,不能用来制备氨气;
C、二氧化硫具有漂白性,和有色物质结合形成不稳定的无色物质,和高锰酸钾溶液反应褪色是利用二氧化硫的还原性;
D、电离平衡常数比较可知,碳酸酸性大于次氯酸,可以在次氯酸钠溶液中通入二氧化碳制备次氯酸.
解答 解:A、苯甲酸的溶解度随温度升高而增大,蒸发结晶析出苯甲酸晶体,过滤不能得到纯净的苯甲酸,应趁热过滤除去苯甲酸中混有的泥沙,叙述Ⅰ正确,Ⅱ错误,故A错误;
B、氯化铵受热易分解,但分解生成的氯化氢和氨气会重新反应生成氯化铵,不能用来制备氨气,叙述Ⅰ正确,Ⅱ错误,无有因果关系,故B错误;
C、二氧化硫具有漂白性,和有色物质结合形成不稳定的无色物质,和高锰酸钾溶液反应褪色是利用二氧化硫的还原性,叙述Ⅰ、Ⅱ均正确,但无有因果关系,故C错误;
D、电离平衡常数比较可知,碳酸酸性大于次氯酸,可以在次氯酸钠溶液中通入二氧化碳制备次氯酸,反应生成次氯酸和碳酸氢钠,叙述Ⅰ和Ⅱ均正确并有因果关系,故D正确;
故选D.
点评 本题考查了铵盐性质、二氧化硫还原性、弱电解质电离平衡的分析判断,主要是物质性质的准确把握,掌握基础是关键,题目难度中等.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
7.下列说法正确的是( )
| A. | 大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 | |
| B. | Na2O2、NH4C1、MgCl2均属于含有共价键的离子化合物 | |
| C. | 乙烯和氯乙烯都可以通过聚合反应得到高分子材料 | |
| D. | 玻璃、水泥和光导纤维的主要成分都是硅酸盐 |
11.如图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液.下列说法不正确的是( )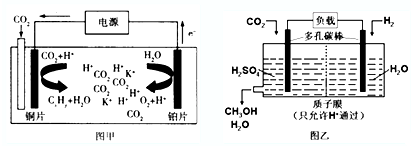

| A. | 甲中铜片作阴极,K+向铜片电极移动 | |
| B. | 甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 | |
| C. | 乙中H2SO4的作用是增强溶液的导电性 | |
| D. | 乙中正极发生的电极反应为CO2+6e-+6H+═CH3OH+H2O |
1.19.2gCu溶于100mL浓度分别为1mol•L-1的HNO3和H2SO4的混合酸中,若产生的气体为NO,最多产生的NO在标准状况下体积为( )
| A. | 2.24L | B. | 1.68L | C. | 3.36L | D. | 1.12L |
8.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液:Na+、NH4+、S2-、NO3- | |
| B. | c(HSO4-)=0.1 mol/L的溶液:K+、Ba2+、HCO3-、Cl- | |
| C. | 滴入少量苯酚显紫色的溶液:Na+、K+、I-、SO42- | |
| D. | 能溶解碳酸钙的溶液:Na+、NH4+、Cl-、Br- |
5.下列关于实验室制取气体所用试剂的组合合理的是( )
| A. | 制Cl2:MnO2、盐酸(稀) | B. | 制H2:硝酸(稀)、Zn | ||
| C. | 制O2:MnO2、H2O2 | D. | 制CO2:硫酸(稀)、CaCO3 |
10.下列说法中,正确的是( )
| A. | 浓硫酸与稀硫酸具有强氧化性 | |
| B. | 某强酸性溶液中含有较多的SO32-、S2- | |
| C. | SO2、H2SO3、H2S都具有还原性 | |
| D. | 加BaCl2溶液生成白色沉淀,原溶液中一定含有SO42- |
