题目内容
【题目】研究发现,NOx和SO2是雾霾的主要成分。
Ⅰ. NOx主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。
已知:N2(g)+O2(g) ![]() 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g) ![]() 2CO2(g) ΔH=-564 kJ·mol-1
2CO2(g) ΔH=-564 kJ·mol-1
(1)2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=_________,该反应在_______下能自发进行(填写:高温或低温或任意温度)
2CO2(g)+N2(g) ΔH=_________,该反应在_______下能自发进行(填写:高温或低温或任意温度)
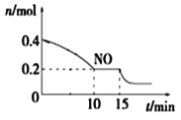
(2)T℃时,将等物质的量的NO和CO充入容积为2 L的密闭容器中,保持温度和体积不变,反应过程(0~15 min)中NO的物质的量随时间变化如上图所示。
①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为p=20MPa,则T℃时该反应的压力平衡常数Kp=_______;平衡后,若保持温度不变,再向容器中充入NO和CO2各0.3mol,平衡将_____(填“向左”、“向右”或“不”)移动。
②15 min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是_____(填序号)
A.增大CO浓度 B.升温 C.减小容器体积 D.加入催化剂
Ⅱ. SO2主要来源于煤的燃烧。燃烧烟气的脱硫减排是减少大气中含硫化合物污染的关键。

已知:亚硫酸:Ka1=2.0×10-2 Ka2=6.0×10-7
(3)请通过计算证明,NaHSO3溶液显酸性的原因:______________________________
(4)如上方图示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为____________________;若通入的NO体积为4.48L(标况下),则另外一个电极通入的SO2质量至少为________g。
【答案】 -744 kJ·mol-1 低温 0.0875(MPa)-1(或7/80(MPa)-1) 不 AC HSO3-的水解常数K=Kw/Ka1=5.0×10-13<Ka2=6.0×10-7(HSO3-的电离常数),所以显酸性 6H++NO+5e-===NH![]() +H2O 32
+H2O 32
【解析】(1)本题考查热化学反应方程式的计算,①N2(g)+O2(g) ![]() 2NO(g),②2CO(g)+O2(g)
2NO(g),②2CO(g)+O2(g) ![]() 2CO2(g),②-①得出:△H=(-564-180)kJ·mol-1=-744kJ·mol-1;△H<0,根据反应方程式,△S<0,根据△G=△H-T△S,当温度处于低温下,能够自发进行;(2)考查化学平衡常数计算、勒夏特列原理,①2NO(g)+2CO(g)
2CO2(g),②-①得出:△H=(-564-180)kJ·mol-1=-744kJ·mol-1;△H<0,根据反应方程式,△S<0,根据△G=△H-T△S,当温度处于低温下,能够自发进行;(2)考查化学平衡常数计算、勒夏特列原理,①2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)
2CO2(g)+N2(g)
起始: 0.4 0.4 0 0
变化: 0.2 0.2 0.2 0.1
平衡: 0.2 0.2 0.2 0.1,各组分的体积分数分别是:2/7、2/7、2/7、1/7,Kp=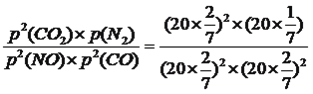 =0.0875;根据①的分析,化学平衡常数K=0.05,再向容器中充入NO和CO2各0.3mol,此时的浓度商为仍为0.05,因此平衡不移动;②15min时,改变某一因素,NO的物质的量减少,说明平衡向正反应方向移动,A、增大CO的浓度,平衡向正反应方向移动,NO的物质的量减小,故A正确;B、正反应是放热反应,升温,平衡向逆反应方向移动,NO的物质的量增大,故B错误;C、减小容器的体积,相当于增大压强,平衡向正反应方向移动,NO物质的量减小,故C正确;D、加入催化剂,化学平衡不移动,故D错误;(3)考查电离平衡常数、水解平衡常数、水的离子积的关系,HSO3-的水解常数K=Kw/Ka1=5.0×10-13<Ka2=6.0×10-7,电离平衡常数大于水解平衡常数,说明溶液显酸性;(4)考查电极反应式的书写、电化学计算,根据电解装置,NO和SO2转化为硫酸铵,说明NO转化成NH4+,即NO在阴极上发生NO+6H++5e-=NH4++H2O;阳极反应式为SO2+2H2O-2e-=4H++SO42-,根据得失电子数目守恒,因此有2NO~10e-~5SO2,求出SO2的质量为4.48×5×64/(2×22.4)g=32g。
=0.0875;根据①的分析,化学平衡常数K=0.05,再向容器中充入NO和CO2各0.3mol,此时的浓度商为仍为0.05,因此平衡不移动;②15min时,改变某一因素,NO的物质的量减少,说明平衡向正反应方向移动,A、增大CO的浓度,平衡向正反应方向移动,NO的物质的量减小,故A正确;B、正反应是放热反应,升温,平衡向逆反应方向移动,NO的物质的量增大,故B错误;C、减小容器的体积,相当于增大压强,平衡向正反应方向移动,NO物质的量减小,故C正确;D、加入催化剂,化学平衡不移动,故D错误;(3)考查电离平衡常数、水解平衡常数、水的离子积的关系,HSO3-的水解常数K=Kw/Ka1=5.0×10-13<Ka2=6.0×10-7,电离平衡常数大于水解平衡常数,说明溶液显酸性;(4)考查电极反应式的书写、电化学计算,根据电解装置,NO和SO2转化为硫酸铵,说明NO转化成NH4+,即NO在阴极上发生NO+6H++5e-=NH4++H2O;阳极反应式为SO2+2H2O-2e-=4H++SO42-,根据得失电子数目守恒,因此有2NO~10e-~5SO2,求出SO2的质量为4.48×5×64/(2×22.4)g=32g。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】硫代硫酸钠(Na2S2O3·5H2O) 俗名“大苏打”。易溶于水,难溶于乙醇,沸点为100℃,酸性或加热条件下易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
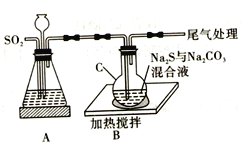
回答下列问题:
(1)装置A可用于观察SO2的生成速率,其中的液体最好选择_____________(填序号)。若装置堵塞使气流不畅,则A中的现象为_______________________________。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)尾气处理可以选择以下装置中的________(填序号)。
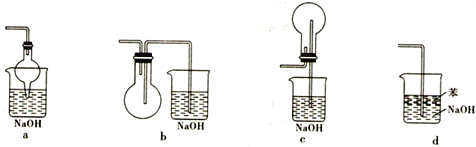
(3)反应过程中若pH值小于7则会降低产率,请用离子方程式解释原因:_________________________。
(4)请写出装置C中发生反应的化学方程式:_________________________。
(5)反应结束后,取C中混合物趁热过滤,取滤液于蒸发皿中, ______________,抽滤,洗涤,低温下干燥得产品。洗涤时要尽量减少产品的损失,其具体操作是_________________________。
(6)为检验制得的产品的纯度,该实验小组称取4g 的产品配制成250mL 硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入20mL 0.0lmol·L-1KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+ S4O62-,实验数据如下表:
实验序号 | 1 | 2 | 3 |
Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.2 |
当滴入最后一滴Na2S2O3溶液时,溶液___________,且半分钟内不变化,则达到终点。计算该产品的纯度是____________________________。


