题目内容
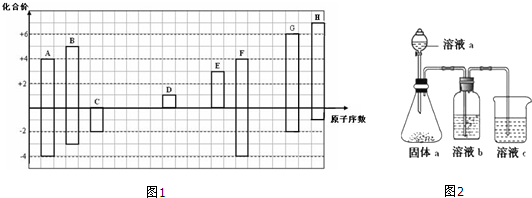
12.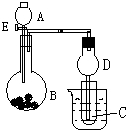 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中:(1)若A为浓硫酸;B为第三周期金属元素的片状单质,在常温下与冷水反应现象不明显;C为品红溶液.观察到品红溶液褪色.则B与浓H2SO4反应化学方程式:Mg+2H2SO4(浓)═MgSO4+SO2↑+2H2O,反应停止后往烧杯中加入沸水,又可观察到试管C中的现象:溶液又呈红色;
(2)若B为Na2CO3溶液,C为C6H5ONa溶液,实验所观察到小试管内溶液由澄清变浑浊,则试管C中化学反应的离子方程式:C6H5O-+H2O+CO2→C6H5OH+HCO3-,然后往烧杯中加入沸水,可观察到试管C中的现象:浑浊变澄清;
(3)若B是生石灰,观察到C溶液先形成沉淀,然后沉淀溶解.当沉淀完全溶解,恰好变澄清时,关闭E.然后往小试管中加入少量葡萄糖溶液,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是氨水(填名称),C是AgNO3(填化学式).
分析 (1)若A为浓硫酸;B为第三周期金属元素的片状单质,在常温下与冷水反应现象不明显,应为Mg;C为品红溶液.观察到品红溶液褪色,说明生成二氧化硫气体;
(2)碳酸酸性比苯酚强,二氧化碳可与苯酚钠溶液反应生成苯酚;
(3)观察到试管壁出现光亮的银镜,说明C中生成银氨溶液,则A应为浓氨水,在生石灰作用下生成氨气,氨气与硝酸银溶液反应生成银氨溶液,银氨溶液与乙醛在加热条件下反应生成银镜.
解答 解:(1)若A为浓硫酸;B为第三周期金属元素的片状单质,在常温下与冷水反应现象不明显,应为Mg;C为品红溶液.观察到品红溶液褪色,说明生成二氧化硫气体,反应的方程式为Mg+2H2SO4(浓)═MgSO4+SO2↑+2H2O,二氧化硫的漂白性具有可逆性,加热可恢复原来的颜色,
故答案为:Mg+2H2SO4(浓)═MgSO4+SO2↑+2H2O;溶液又呈红色;
(2)碳酸酸性比苯酚强,二氧化碳可与苯酚钠溶液反应生成苯酚,方程式为C6H5O-+H2O+CO2→C6H5OH+HCO3-,加热时,苯酚的溶解度增大,溶于水,可观察到溶液变澄清,
故答案为:C6H5O-+H2O+CO2→C6H5OH+HCO3-;浑浊变澄清;
(3)观察到试管壁出现光亮的银镜,说明C中生成银氨溶液,则A应为浓氨水,在生石灰作用下生成氨气,氨气与硝酸银溶液反应生成银氨溶液,银氨溶液与乙醛在加热条件下反应生成银镜,
故答案为:氨水; AgNO3.
点评 本题考查较为综合,涉及物质的性质探究以及制备等知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的原理、方法,难度不大.

练习册系列答案
相关题目
2.下列反应中前者属于取代反应,后者属于加成反应的是( )
| A. | 甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 苯与硝酸在一定条件下反应生成硝基苯;乙烯与溴的四氯化碳溶液反应 | |
| C. | 乙烯与水生成乙醇的反应 | |
| D. | 在苯中滴入溴水,水层褪色;乙烯与溴水反应 |
3.化学与生活密切相关,下列有关说法正确的是( )
| A. | 油脂、乙酸乙酯都属于酯类,水解后都会生成乙醇 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| C. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
4.下列各组中互为同位素的是( )
| A. | D2O和H2O | B. | 235U和238U | C. | 红磷和白磷 | D. | SO2和SO3 |
1.下列表示物质结构的化学用语或模型图正确的是( )
| A. | Cl原子结构示意图: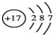 | B. | H2O2的电子式: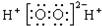 | ||
| C. | HClO的结构式H-O-Cl | D. | 14C的原子结构示意图: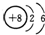 |
2.阅读下表中部分短周期主族元素的相关信息,请回答:
(1)元素T与X按原子个数比1:1形成的化合物B的电子式为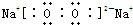 ,该化合物中所含的化学键有离子键、共价键(填化学键名称).
,该化合物中所含的化学键有离子键、共价键(填化学键名称).
(2)单质T与冷水反应的化学方程式为2Na+2H2O═2NaOH+H2↑
(3)将T的最高价氧化物对应水化物的溶液逐滴加入到Y与Z形成的化合物的溶液中,直至过量(边滴加边振荡),写出此过程中发生反应的离子方程式Al3++4OH-═AlO2-+2H2O、Al3++3AlO2-+6H2O═4Al(OH)3↓.
| 元素代号 | 相关信息 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期的所有金属离子中,Y的离子半径最小 |
| Z | Z与Y同周期,是所在周期中原子半径最小的元素 |
| T | T的单质能与冷水剧烈反应,生成的强碱电离出两种电子数相等的阴、阳离子 |
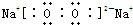 ,该化合物中所含的化学键有离子键、共价键(填化学键名称).
,该化合物中所含的化学键有离子键、共价键(填化学键名称).(2)单质T与冷水反应的化学方程式为2Na+2H2O═2NaOH+H2↑
(3)将T的最高价氧化物对应水化物的溶液逐滴加入到Y与Z形成的化合物的溶液中,直至过量(边滴加边振荡),写出此过程中发生反应的离子方程式Al3++4OH-═AlO2-+2H2O、Al3++3AlO2-+6H2O═4Al(OH)3↓.
 ,其所含化学键类型为离子键.
,其所含化学键类型为离子键.