题目内容
【题目】人类生活离不开化学,以下是补铁剂和胃药的两张标签的部分信息。
硫酸亚铁片 英文名:Ferrous Sulfate Tablets 本品含硫酸亚铁(FeSO4·7H2O)应为标示量的95.0%~110.0% | 氢氧化铝片 英文名:Aluminium Hydroxide Tablets |
(主要成分)糖衣、碳酸镁、氢氧化铝、淀粉 | |
(性状)本品为糖衣,除去糖衣后显淡绿色 | (适应症)能缓解胃酸过多 |
(鉴别)取本品,除去糖衣,称取适量(约相当于硫酸亚铁片0.2g),加稀盐酸1滴与水20mL,振摇使硫酸亚铁溶解,过滤,滤液进行亚铁盐与硫酸盐的鉴别反应 | (用法用量)成人:口服,一次0.6~0.9g(一次2~3片),一日3次,餐前1小时服用 |
(详细用法)详见说明书 |
I、根据“硫酸亚铁片”标签回答问题:
(1)硫酸亚铁片溶于水后溶液的颜色是_______________。
(2)硫酸盐中检验![]() 的离子反应方程式是______________________________________。
的离子反应方程式是______________________________________。
(3)鉴别中,“加稀盐酸1滴”的作用是__________________________________________。
(4)检验硫酸亚铁片是否被氧化的方法是________________________________________。
II、根据“氢氧化铝片”标签回答问题:
(1)能缓解胃酸过多的成分是__________________________________________。
(2)氢氧化铝可作为治疗胃酸过多的内服药,这是利用了氢氧化铝的______________。
A. 酸性 B. 碱性 C. 两性 D. 氧化性
(3)写出氢氧化铝的电离方程式:_____________________________________________。
【答案】淡绿色 SO42+Ba2+=BaSO4↓ 抑制Fe2+水解 取适量硫酸亚铁片,溶于水中配成溶液。取少量溶液,滴加数滴KSCN溶液,观察颜色变化。若无明显现象,说明硫酸亚铁片未被氧化 碳酸镁、氢氧化铝 B ![]()
![]()
![]()
【解析】
I (1)亚铁离子在溶液中呈浅绿色;
(2)硫酸根离子的检验:向溶液中加入盐酸使之酸化,再加入BaCl2溶液,有白色沉淀产生;
(3)亚铁离子在水溶液中易发生水解;
(4)硫酸亚铁中的亚铁离子具有较强还原性,容易被氧化成铁离子,可以通过加入硫氰化钾溶液检验是否存在铁离子,进行判断硫酸亚铁是否变质;
II(1) 该药片能缓解胃酸过多,胃酸的主要成分是盐酸,能与盐酸反应的物质为有效成分;
(2)氢氧化铝是两性氢氧化物,即可与强酸反应又可与强碱反应,胃酸的主要成分是盐酸;
(3)氢氧化铝是两性氢氧化物,既可以酸式电离也可以碱式电离。
I (1)亚铁离子在溶液中呈浅绿色,硫酸亚铁片溶于水后产生亚铁离子,溶液的颜色是浅绿色;
(2) 硫酸根离子的检验:向溶液中加入盐酸使之酸化,再加入BaCl2溶液,有白色沉淀产生,方程式为SO42+Ba2+=BaSO4↓;
(3) 亚铁离子在水溶液中易水解,加盐酸增大氢离子浓度可以抑制水解;
(4) 硫酸亚铁若是变质,亚铁离子会被氧化成铁离子,所以可使用KSCN溶液检验,加入硫氰化钾,若溶液变成红色,证明硫酸亚铁已经变质,若溶液没有变成红色,证明硫酸亚铁没有变质;
II(1)该药片能缓解胃酸过多,胃酸的主要成分是盐酸,MgCO3、Al(OH)3与盐酸反应是有效成分;
(2)氢氧化铝是两性氢氧化物,即可与强酸反应又可与强碱反应,胃酸的主要成分是盐酸,可与氢氧化铝反应,利用了氢氧化铝的碱性,答案选B;
(3)氢氧化铝是两性氢氧化物,既可以酸式电离也可以碱式电离,电离方程式为:![]()
![]()
![]() 。
。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】某兴趣小组用镀锌铁皮按下列流程制备七水合硫酸锌(ZnSO4·7H2O)
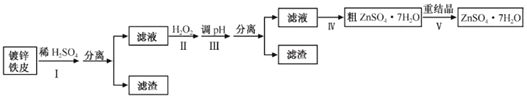
相关信息如下:
①金属离子形成氢氧化物沉淀的相关pH范围。
金属离子 | pH | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Zn2+ | 5.4 | 8.2 |
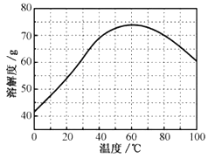
②ZnSO4的溶解度(物质在100g水中溶解的质量)随温度变化曲线。请回答:
(1)①镀锌铁皮上的油污可用Na2CO3溶液去除,理由是__。
②步骤Ⅰ可用于判断镀锌层完全反应的实验现象是__。
(2)步骤Ⅱ须加入过量H2O2理由是__。
(3)步骤Ⅲ,合适的pH范围是__。
(4)步骤Ⅳ,需要用到下列所有操作:a.蒸发至溶液出现晶膜,停止加热;b.在60℃蒸发溶剂;c.冷却至室温;d.在100℃蒸发溶剂;e.过滤。
请给出上述操作的正确顺序__。(操作可重复使用)
(5)步骤Ⅴ,某同学采用不同降温方式进行冷却结晶,测得ZnSO47H2O晶体颗粒大小分布如图所示。根据该实验结果,为了得到颗粒大小相对均一的较大晶粒,宜选择__方式进行冷却结晶。
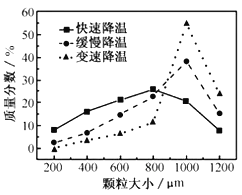
A.快速降温 B.缓慢降温 C.变速降温
(6)①ZnSO47H2O产品的纯度可用配位滴定法测定。
下列关于滴定分析,正确的是__。
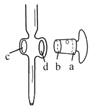
A.图中,应将凡士林涂在旋塞的a端和旋塞套内的c端
B.滴定前,锥形瓶和滴定管均须用标准溶液润洗
C.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
D.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
E.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得的体积比实际消耗的小
②图中滴定终点是的读数是___mL。