题目内容
7.下列有关氢气与氯气反应的叙述中,不正确的是( )| A. | 纯净的氢气在氯气里安静地燃烧,发出苍白色火焰 | |
| B. | 氢气与氯气反应生成的氯化氢气体与空气里的水蒸气结合,呈白雾状 | |
| C. | 氢气与氯气混合后,光照发生爆炸 | |
| D. | 氢气与氯气的反应是化合反应,是氧化还原反应,且有电子得失 |
分析 A.氢气在氯气中燃烧,发出苍白色火焰;
B.氯气和氢气反应生成的氯化氢极易溶于水分析;
C.氯气和氢气混合光照发生爆炸反应完全;
D.氢气与氯气反应属于氧化还原反应,存在电子偏移.
解答 解:A.氢气在氯气中燃烧生成氯化氢气体,发出苍白色火焰,故A正确;
B.氯气和氢气反应生成的氯化氢极易溶于水,遇到空气中的水蒸气会形成白雾为盐酸小液滴,故B正确;
C.氯气和氢气混合光照发生爆炸反应完全生成氯化氢气体,故C正确;
D.氢气与氯气的反应是化合反应,是氧化还原反应,且有电子偏移,故D错误;
故选:D.
点评 本题考查了氢气与氯气的反应,熟悉氯气的性质,明确氢气与氯气反应条件及产物性质是解题关键,题目难度不大.

练习册系列答案
相关题目
15.下列指定物质的所占有体积约为最大的是( )
| A. | 标准状况下56g铁原子 | B. | 20℃、101kPa时36.5gHCl | ||
| C. | 标准状况下6.02×1023个NH3 | D. | 标准状况下1molC2H5OH |
2.NA表示阿伏加德罗常数的数值,下列有关说法错误的是( )
| A. | 在标准状况下,33.6L SO3中含有的原子数目为6NA | |
| B. | 1L 1mol/L醋酸溶液中,H+数目小于NA | |
| C. | 等体积、等质量的CO和N2具有相同的电子数目 | |
| D. | 1mol Fe与足量的氯气反应转移的电子数目为3NA |
16.关于电解的下列叙述中,正确的是( )
| A. | 惰性电极电解稀Na2SO4水溶液时,分别在两极滴加一滴石蕊,一段时间后,阳极附近溶液变蓝,阴极附近溶液变红 | |
| B. | 为使反应Cu+2H2O═Cu(OH)2↓+H2↑发生,可用铜片作阴、阳电极,电解NaCl水溶液 | |
| C. | 电解法精炼粗铜时,应使粗铜与电源正极相连,过程中电解质溶液中Cu2+浓度不变 | |
| D. | 惰性电极电解MgCl2溶液的总反应方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- |
17.NA 表示阿伏加德罗常数,则下列说法正确的是( )
| A. | 1 mol Mg 原子变成 Mg2+时失去的电子数为2 NA | |
| B. | 标准状况下,11.2 L H2O所含的电子数为5 NA | |
| C. | 常温常压下,16g O2 与16gO3含有的原子数为相同 | |
| D. | 0.1 mol/L K2SO4 溶液中含有 K+为0.2 NA |

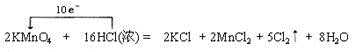 ,在该反应中氧化剂是KMnO4,氧化剂和还原剂的物质的量之比为1:5,产生标准状况下33.6LCl2时,转移电子的物质的量为3mol.
,在该反应中氧化剂是KMnO4,氧化剂和还原剂的物质的量之比为1:5,产生标准状况下33.6LCl2时,转移电子的物质的量为3mol.