题目内容
12.(1)反应KMnO4+HCl-KCl+MnCl2+Cl2↑+H2O未配平,请写出配平好的该反应方程式并表示电子转移的方向和数目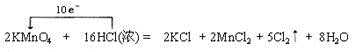 ,在该反应中氧化剂是KMnO4,氧化剂和还原剂的物质的量之比为1:5,产生标准状况下33.6LCl2时,转移电子的物质的量为3mol.
,在该反应中氧化剂是KMnO4,氧化剂和还原剂的物质的量之比为1:5,产生标准状况下33.6LCl2时,转移电子的物质的量为3mol.(2)将NaOH溶液滴加到FeSO4溶液中产生的现象是产生白色沉淀迅速变为灰绿色,最终变为红褐色,本实验应将胶头滴管伸入到液面以下,这样做的目的是防止Fe(OH)2被氧化,为了达到此目的还可以采取的措施有液封或将蒸馏水煮沸除氧或通保护气(任写一种).
分析 (1)反应物KMnO4中Mn元素的化合价降低,HCl中Cl的化合价升高,氧化还原反应中转移的电子数目=化合价升高的数目=化合价降低的数目,化合价降低元素所在的反应物是氧化剂,还原剂在反应中被氧化发生氧化反应;
(2)NaOH溶液与FeSO4溶液反应生成氢氧化亚铁白色沉淀,氢氧化亚铁易被氧化为氢氧化铁,为了防止被氧化要排除氧气.
解答 解:(1)根据得失电子守恒和原子守恒配平方程式为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,反应中KMnO4中Mn元素的化合价降低,HCl中Cl的化合价升高,氧化剂是高锰酸钾,还原剂是盐酸,氧化剂和还原剂的物质的量之比为为1:5,产生标准状况下33.6LCl2即1.5mol,转移电子为3mol;
故答案为: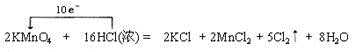 ;KMnO4;1:5;3mol;
;KMnO4;1:5;3mol;
(2)NaOH溶液与FeSO4溶液反应生成氢氧化亚铁白色沉淀,氢氧化亚铁易被氧化为氢氧化铁,其现象为产生白色沉淀迅速变为灰绿色,最终变为红褐色,为了防止被氧化要排除氧气,可以将胶头滴管伸入到液面以下或液封或将蒸馏水煮沸除氧或通保护气;
故答案为:产生白色沉淀迅速变为灰绿色,最终变为红褐色;防止Fe(OH)2被氧化;液封或将蒸馏水煮沸除氧或通保护气.
点评 本题考查学生氧化还原反应中的基本概念以及电子转移知识、铁的化合物的制备和性质,侧重于考查学生对基础知识的应用能力,注意把握氧化还原反应中电子转移的表示方法.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
2.在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
(已知N2(g)+3H2(g)═2NH3(g);△H=-92.4kJ•mol-1),下列说法正确的是( )
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol N2、3mol H2 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 气体密度 | ρ1 | ρ2 |
| 反应物转化率 | α1 | α2 |
| A. | c1<c2<2c1 | B. | a+b>92.4 | C. | α1+α 2=1 | D. | ρ2=3ρ1 |
20.下列表述不正确的是( )
| A. | 人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3 | |
| B. | 硅是制造太阳能电池的常用材料 | |
| C. | 四氧化三铁俗称铁红,可用于作油漆、红色涂料 | |
| D. | 分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液 |
7.下列有关氢气与氯气反应的叙述中,不正确的是( )
| A. | 纯净的氢气在氯气里安静地燃烧,发出苍白色火焰 | |
| B. | 氢气与氯气反应生成的氯化氢气体与空气里的水蒸气结合,呈白雾状 | |
| C. | 氢气与氯气混合后,光照发生爆炸 | |
| D. | 氢气与氯气的反应是化合反应,是氧化还原反应,且有电子得失 |
17.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生的反应有Zn+Cu2+=Zn2++Cu、Zn+2H+=Zn2++H2↑.(离子方程式)
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了原电池,写出该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑.
(3)要加快上述实验中气体产生的速率,还可采取的措施有BC.
A.将稀硫酸换成浓硫酸 B.适当升高温度
C.用锌粉代替锌粒 D.增加上述稀硫酸的用量
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
(1)上述实验中发生的反应有Zn+Cu2+=Zn2++Cu、Zn+2H+=Zn2++H2↑.(离子方程式)
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了原电池,写出该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑.
(3)要加快上述实验中气体产生的速率,还可采取的措施有BC.
A.将稀硫酸换成浓硫酸 B.适当升高温度
C.用锌粉代替锌粒 D.增加上述稀硫酸的用量
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
1.下列下说法正确的是( )
| A. | 化学键断裂时吸收能量,形成时放出能量 | |
| B. | 燃烧热是1mol可燃物完全燃烧释放的能量 | |
| C. | 中和热是稀酸与稀碱反应生成1molH2O释放的能量 | |
| D. | 燃料电池能将全部化学能转化为电能 |

 名称是3,5-二甲基庚烷.
名称是3,5-二甲基庚烷.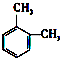 名称是1,2-二甲苯.
名称是1,2-二甲苯.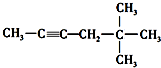 名称是5,5-二甲基-2-己炔.
名称是5,5-二甲基-2-己炔. 名称是4-甲基-1-戊烯.
名称是4-甲基-1-戊烯.