题目内容
【题目】下列关于浓硫酸特性的叙述不正确的是
A. 浓硫酸具有吸水性、脱水性和强氧化性等特性
B. 浓硫酸能吸收气体中的水蒸气,常作氨气、二氧化硫等气体的干燥剂
C. 浓硫酸可以吸收固体中的湿存水、结晶水合物中的结晶水
D. 在反应C12H22O11![]() 12C+11H2O,浓硫酸作脱水剂
12C+11H2O,浓硫酸作脱水剂
【答案】B
【解析】
浓硫酸具有吸收现成的水(如气体中、液体中的水分子,以及固体中的结晶水等)的性能,表现浓硫酸的吸水性,浓硫酸可将许多有机物中的氢和氧原子按水分子的组成比例脱去,表现浓硫酸的脱水性,常温下,浓硫酸可使铁、铝等金属钝化.加热时,大多数金属都能被浓硫酸氧化为最高价态.此类反应生成相应的金属硫酸盐、二氧化硫和水,表现浓硫酸的强氧化性,通常情况下,浓硫酸可做干燥剂,但由于浓硫酸具有酸性和强氧化性,所以不能干燥碱性气体和还原性气体,所以不能干燥NH3、H2S等,可以干燥SO2、O2、N2等,故B错误;
本题答案为B。

 优质课堂快乐成长系列答案
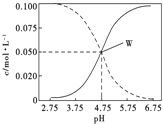
优质课堂快乐成长系列答案【题目】SO2是国内外允许使用的一种食品添加剂,在食品工业中发挥着护色、防腐、漂白和抗氧化的作用。我国对于SO2的添加量有明确规定(如图所示)。

某研究小组用图装置对市售黄花菜中的SO2进行测定。其中,溶液X为黄花菜进行充分浸泡后所得浅黄色浸泡液,Y为加入的试剂。(Y的浓度及体积均未标出)查阅资料发现,在水溶液中正四价硫元素主要以SO32-形式存在,且SO2与SO32-化学性质相似。因此,该小组同学将SO2的测定问题转化为溶液中SO32-的测定。
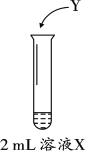
(1)结合化学知识解释浸泡液X中存在SO32-的原因是______。
(2)甲同学预测可用Na2S溶液验证X中是否含有SO32-,该预测应用的是Na2S的______性。查阅资料发现该反应较为复杂,因此未做进一步验证。
(3)乙同学为验证X中是否含有SO32-,进行了实验i:
实验序号 | 试剂Y | 现象 |
i | 酸性KMnO4溶液 | ① |
根据实验i 的现象得出结论:X中含有SO32-。实验i的现象是________,SO32-在反应后转化为_________。
(4)丙同学认为也可以用H2O2溶液来验证X中是否含有SO32-,进行了实验ii:
实验序号 | 操作 | 现象 |
ii | a.向X中加入适量H2O2溶液,振荡 | 无明显现象 |
b.继续滴加 ,振荡 | 无明显现象 | |
c.再滴加 ,振荡 | 白色沉淀 |
通过实验ii可证明X中含有SO32-,写出操作b、c中滴加试剂的化学式____、 _____ 。
(5)丁同学认为丙的实验方案不严谨,设计了对比实验ⅲ,证明了X中含有SO32-。实验ⅲ的方案是(从操作、现象、结论方面描述)________ 。
(6)为测定市售黄花菜中SO2含量,进行实验ⅳ:
实验序号 | 操作 |
ⅳ | a.将50克黄花菜研碎,用一定浓度氢氧化钠溶液浸泡; b.加稀硫酸酸化; c.加入淀粉指示剂; d.用浓度为0.01mol/L的I2溶液滴定,消耗0.01mol/L的I2溶液5.00 mL。 |
查阅资料发现:碘元素的常见价态有-1,0,+1,+3,+5,+7。
① 将黄花菜用氢氧化钠溶液浸泡的目的是(用化学方程式表示)__________。
② 写出滴定反应的化学方程式____________。
③ 该市售黄花菜中SO2残留量是________毫克/千克。