题目内容
【题目】氢气是一种理想的“绿色能源”,利用氢能需要选择合适的储氢材料。目前正在研究和使用的储氢材料有镁系合金、稀土系合金等。
(1)已知,Mg(s) +H2(g)==MgH2(s) △H=-74.5kJ/mol
Mg2Ni(s) + 2H2(g)==Mg2NiH4(s) △H=-64.4kJ/mol
MgNi(s)+ 2MgH2(s)==2Mg(s)+ Mg2NiH4(s) △H=____kJ/mol。
(2)储氢材料Mg(AlH4)2在110~200℃的反应为:Mg(AlH4)2==MgH2+2Al+3H2↑。反应中每转移3mol电子时,产生的H2在标准状况下的体积为_____________L。
(3)镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g) ![]() LaNi5H6(s) △H<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_________(填字母编号)。
LaNi5H6(s) △H<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_________(填字母编号)。
a.增加LaNi5H6(s)的量 b.升高温度 c.减小压强 d.使用催化剂
(4)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:![]()

①某温度下,向恒容密闭容器中加入环己烷,起始浓度为amol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=_____________(用含a、b的代数式表示)。
②一定条件下,下图装置可实现有机物的电化学储氢(忽略其它有机物)。A是电源的__________极(填“正”或“负”);电解过程中产生的气体F为________(填化学式):电极D上发生的电极反应为____________。
【答案】 +84.6 33:6 b c 27b4/(a-b) 负 O2 C6H6+6H++6e-=C6H12
【解析】(1)本题考查热化学反应方程式的计算,①Mg(s) +H2(g)=MgH2(s),②Mg2Ni(s)+2H2(g)=Mg2NiH4(s),根据目标方程式,②-①×2,△H=+84.6kJ·mol-1;(2)考查氧化还原反应,根据反应方程式,Al的化合价降低,一部分H的化合价升高,一部分H不变,因此生成3molH2,转移电子物质的量为6mol,转移3mol电子,生成氢气物质的量为1.5mol,即氢气的体积为1.5×22.4L=33.6L;(3)本题考查勒夏特列原理,a、LaNi5H6为固体,浓度视为常数,对化学平衡移动无影响,故a错误;b、正反应是放热反应,升高温度,平衡向逆反应方向进行,释放出氢气,故b正确;c、减小压强,平衡向正反应方向移动,释放出氢气,故c正确;d、催化剂对化学平衡的移动无影响,故d错误;(4)考查平衡常数计算、电解原理、电极反应式的书写,①
![]()
起始: a 0 0
变化: b b 3b
平衡: a-b b 3b,化学平衡常数K= =27b4/(a-b);②根据装置图,C6H6→C6H12,C的化合价降低,即电极D为阴极,A是电源的负极,阳极上发生4OH--4e-=O2↑+2H2O,气体F为O2,电极D电极反应式为C6H6+6H++6e-=C6H12。
=27b4/(a-b);②根据装置图,C6H6→C6H12,C的化合价降低,即电极D为阴极,A是电源的负极,阳极上发生4OH--4e-=O2↑+2H2O,气体F为O2,电极D电极反应式为C6H6+6H++6e-=C6H12。

【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
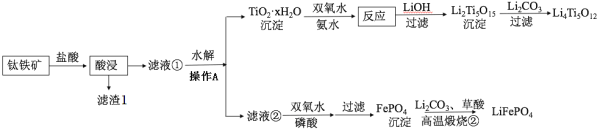
回答下列问题:
(1)滤渣1为_______________,操作A为_________________,向滤液②中加入双氧水的作用是___________________________________。
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因_______________________________。
(4)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?_____________________________________________(列式计算)。FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
【题目】下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25℃)。
电解质 | 电离方程式 | 电离常数K或Ksp |
CH3COOH | CH3COO | 1.76×10-5 |
H2CO3 | H2CO3 HCO3- | K1=4.31×10-7 K2=5.61×10-11 |
C6H5OH | C6H5OH | 1.1×10-10 |
H3PO4 | H3PO4 H2PO4- HPO42- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
NH3·H2O | NH3·H2O | 1.76×10-5 |
BaSO4 | BaSO4(s) | 1.07×10-10 |
BaCO3 | BaCO3(s) | 2.58×10-9 |
回答下列问题:
(1)由上表分析,若①CH3COOH,②HCO3-,③C6H5OH,④H2PO4-均可看做酸,则它们酸性由强到弱的顺序为_____________(填编号)。
(2)写出C6H5OH与Na3PO4反应的离子方程式_______________________________。
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)____c(NH4+)(填“>”、“=”或“<”)。
(4)25℃时,向10mL0.01mol/L苯酚溶液中滴加VmL0.01mol/L氨水,混合液中粒子浓度关系正确的是__________(填字母序号)。
A.若混合液pH>7,则V≥10
B.若混合液 pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10mL0.01mol/L苯酚溶液中水的电离程度
D.V= 5时,2c(NH3·H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应,水解反应的化学平衡常数称为水解常数(用Kb表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:____________。
(6)I,如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:

①T1______T2(填“>”、“=”或‘‘<”),T2温度时 Ksp(BaSO4)=_______________;
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是______(填字母序号)。
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a,b之间的某一点(不含a,b)
D.升温可使溶液由b点变为d点
II.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理_____次。[提示:BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq)]
BaCO3(s)+SO42-(aq)]