��Ŀ����
10�������廯����Aֻ��������λȡ��������һ������������ͼ��ʾת����ϵ�����У�1mol C��Na��ȫ��Ӧ����1mol H2����1mol C��NaHCO3��ȫ��Ӧ��Ҳ����1mol���壬E����ʹ������Ȼ�̼��Һ��ɫ��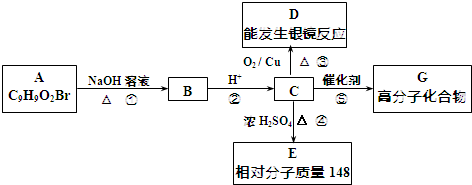
��1��D�����еĺ���������������ȩ�����Ȼ���A�Ľṹ��ʽ��
 ��
����2����Ӧ�ܵĻ�����������ȥ��Ӧ����Ӧ�ٵĻ�ѧ����ʽ��
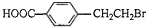 +2NaOH$��_{��}^{ˮ}$
+2NaOH$��_{��}^{ˮ}$ +NaBr+H2O����Ӧ�ݵĻ�ѧ����ʽ��
+NaBr+H2O����Ӧ�ݵĻ�ѧ����ʽ�� ��
����3������C��E�Ļ����n mol���ڿ�������ȫȼ������O2224nL����״������
��4����Cȡ����λ����ͬ��������FeCl3��Һ��ɫ�����ܷ���ˮ�ⷴӦ��ͬ���칹��ṹ��ʽΪ��
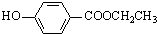 ��
��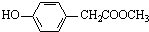 ������4�֣�
������4�֣�
���� 1molC��Na��ȫ��Ӧ����1molH2����1molC��NaHCO3��ȫ��Ӧ��Ҳ����1mol���壬˵��C�к���1��-COOH��1��-OH����λ�ڶ�λλ�ã���C���������ܷ���������Ӧ�����A�Ľṹ�ص�ͷ���ʽ��֪CӦΪ ����AΪ
����AΪ ��BΪ
��BΪ ��DΪ
��DΪ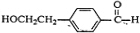 ��E����ʹ������Ȼ�̼��Һ��ɫ��˵����̼̼˫����C��Ũ���������·�����ȥ��Ӧ����E��ӦΪ
��E����ʹ������Ȼ�̼��Һ��ɫ��˵����̼̼˫����C��Ũ���������·�����ȥ��Ӧ����E��ӦΪ ������Է�������Ϊ148��C�к���-OH��-COOH���ɷ������۷�Ӧ���ɸ߷��ӻ��������л���Ľṹ�����ʽ����⣮
������Է�������Ϊ148��C�к���-OH��-COOH���ɷ������۷�Ӧ���ɸ߷��ӻ��������л���Ľṹ�����ʽ����⣮
��� �⣺1molC��Na��ȫ��Ӧ����1molH2����1molC��NaHCO3��ȫ��Ӧ��Ҳ����1mol���壬˵��C�к���1��-COOH��1��-OH����λ�ڶ�λλ�ã���C���������ܷ���������Ӧ�����A�Ľṹ�ص�ͷ���ʽ��֪CӦΪ ����AΪ
����AΪ ��BΪ
��BΪ ��DΪ
��DΪ ��E����ʹ������Ȼ�̼��Һ��ɫ��˵����̼̼˫����C��Ũ���������·�����ȥ��Ӧ����E��ӦΪ
��E����ʹ������Ȼ�̼��Һ��ɫ��˵����̼̼˫����C��Ũ���������·�����ȥ��Ӧ����E��ӦΪ ��
��
��1�������Ϸ��ӿ�֪��DΪ ������ȩ�����Ȼ���A�Ľṹ��ʽ��
������ȩ�����Ȼ���A�Ľṹ��ʽ�� ��
��
�ʴ�Ϊ��ȩ�����Ȼ��� ��
��
��2����Ӧ��ΪC����ȥ��Ӧ��CΪ ������-OH��-COOH����Ӧ��ΪA�ļ���ˮ���Լ��Ȼ����кͣ���Ӧ�Ļ�ѧ����ʽΪ��
������-OH��-COOH����Ӧ��ΪA�ļ���ˮ���Լ��Ȼ����кͣ���Ӧ�Ļ�ѧ����ʽΪ�� +2NaOH$��_{��}^{ˮ}$
+2NaOH$��_{��}^{ˮ}$ +NaBr+H2O����Ӧ��ΪC�������۷�Ӧ���ɸ߷��ӻ������Ӧ�ķ���ʽΪ
+NaBr+H2O����Ӧ��ΪC�������۷�Ӧ���ɸ߷��ӻ������Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ����ȥ�� +2NaOH$��_{��}^{ˮ}$
+2NaOH$��_{��}^{ˮ}$ +NaBr+H2O��
+NaBr+H2O�� ��
��
��3��CΪ ������ʽΪC9H10O3��EΪ
������ʽΪC9H10O3��EΪ ������ʽΪC9H8O2�������ʵ���ʱ���������������ʵ�����ͬ�������nmol���ڿ�������ȫȼ������O2����9+$\frac{8}{4}$-$\frac{2}{2}$��nmol=10nmol��9+$\frac{10}{4}$-$\frac{3}{2}$��nmol=10nmol�������Ϊ10nmol��22.4L/mol=224n��
������ʽΪC9H8O2�������ʵ���ʱ���������������ʵ�����ͬ�������nmol���ڿ�������ȫȼ������O2����9+$\frac{8}{4}$-$\frac{2}{2}$��nmol=10nmol��9+$\frac{10}{4}$-$\frac{3}{2}$��nmol=10nmol�������Ϊ10nmol��22.4L/mol=224n��
�ʴ�Ϊ��224n��
��4����Cȡ����λ����ͬ��������FeCl3��Һ��ɫ��˵�����з��ǻ������ܷ���ˮ�ⷴӦ��˵��������������Ӧ��ͬ���칹����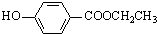 ��
��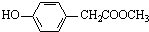 ��
�� �����Գ������е��������4�֣�
�����Գ������е��������4�֣�
�ʴ�Ϊ��4��
���� ���⿼���л�����ƶϣ���Ŀ�Ѷ��еȣ�����ע����ݸ��������Ϣ����CΪ�ƶϸ����ͻ�ƿڣ��ѵ���ͬ���칹����жϣ�ע����������Ϣ�Լ��ж�ͬ���칹��ķ�����

 ��������ϵ�д�
��������ϵ�д�| A�� | ��ˮ���ȣ�KW����pH���� | |
| B�� | ��ˮ�м���������NaOH���壬ƽ�������ƶ���c��OH-������ | |
| C�� | ��ˮ�м���������NH4Cl���壬ƽ�������ƶ�����Һ�ʼ��� | |
| D�� | ��0.1mol/L�Ĵ�����Һ�м���һ�����Ĵ����ƾ��壬��Һ�е�c��OH-������KW���� |
| A�� | C4H8O3�Ľṹ��ʽΪHOCH2CH2CH2COOH | |
| B�� | C4H8O3�Ľṹ��ʽΪCH3CH��OH��CH2COOH | |
| C�� | C4H8O3Ϊ��-�ǻ����� | |
| D�� | C4H8O3Ϊ�ǻ��������� |
| A�� | ������������Һ�м�����������������Һ��NH4++OH-�TNH3•H2O | |
| B�� | �������������м���������ϡ���Fe��OH��2+2H+�TFe2++2H2O | |
| C�� | FeSO4��Һ�ڿ����з��ñ��ʣ�4Fe2++O2+2H2O�T4Fe3++4OH- | |
| D�� | ����SO2ͨ���䰱ˮ�У�SO2+NH3•H2O=HSO3-+NH4+ |
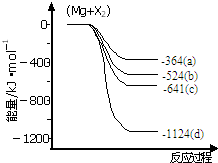
| A�� | ������NA��ˮ�������ӷ�Ӧ��Ϊ��H0�����H0����H | |
| B�� | ����20NA������ת��ʱ���ų�2600kJ ���� | |
| C�� | ����4NA��̼�����õ��Ӷ�����ʱ���ų�1300kJ���� | |
| D�� | ������ӦΪ���ȷ�Ӧ |
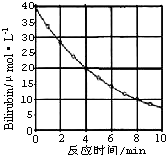 ������Bilirubin��һ�������Ĺ������·����ֽⷴӦ����Ӧ��Ũ���淴Ӧʱ��仯��ͼ��ʾ�����㣺
������Bilirubin��һ�������Ĺ������·����ֽⷴӦ����Ӧ��Ũ���淴Ӧʱ��仯��ͼ��ʾ�����㣺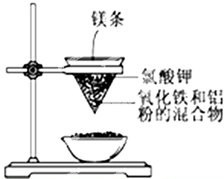
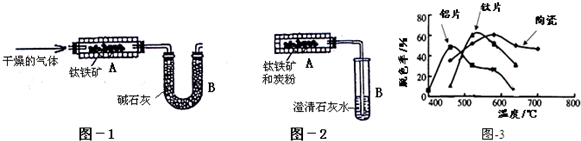
 þ��������й㷺��;����ش��й�þ���������⣺
þ��������й㷺��;����ش��й�þ���������⣺