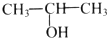��Ŀ����
3�����ᣨH2C2O4�����������������������ܹ��������·�Ӧ��2KMnO4+5H2C2O4+3H2SO4�T2MnSO4+10CO2��+K2SO4+8H2O��һ�����Ļ����Һ������KMnO4Ϊ4.0mL 0.2mol•L-1��H2C2O4Ϊ2.0mL 0.5mol•L-1����̽����ͬ�����Ի�ѧ��Ӧ���ʵ�Ӱ�죮�ı���������£�| ��� | 10%�������/mL | �¶�/�� | �������� |
| �� | 2 | 20 | |
| �� | 2 | 20 | 10�α���MnSO4��Һ |
| �� | 2 | 30 | |
| �� | 1 | 30 | 1mL����ˮ |
��2������5���ӷ�Ӧ��ʵ����в�����ȫ���ģ�������ƽ����Ӧ����Ϊ0.025mol/��L•min����
��3����Ӧ���ɵ�CO2���������ϳɼ״���CH3OH����CO2��g��+3H2��g���TCH3OH��g��+H2O��g����
�÷�Ӧ�Ƿ��ȷ�Ӧ������1mol CO2�еĻ�ѧ����������Q1kJ������1mol H2�еĻ�ѧ����������Q2kJ���γ�1mol CH3OH�еĻ�ѧ���ͷ�����Q3kJ���γ�1mol H2O�еĻ�ѧ���ͷ�����Q4kJ����������£�����1mol CH3OH�ų�������Ϊ��3Q3+Q4-3Q2-Q1��kJ ����Q1��Q2��Q3��Q4�ļ���ʽ��ʾ����
��4����һ�������£��ܱ������н��еķ�ӦCO2��g��+3H2��g���TCH3OH��g��+H2O��g��
�ﵽ��ѧƽ��״̬������˵����ȷ����B������ţ���
A�������ʵ�Ũ�����
B������3mol H2��ͬʱ����1mol CH3OH
C����Ӧ�ﵽƽ��ʱ�������¶ȷ�Ӧ���ʲ��䣮
���� ��1�����ݶ��������б�����Ψһ�Խ����жϣ��磺�о������Ի�ѧ��Ӧ���ʵ�Ӱ�죬���˴��������ͬ������������ȫ��ͬ������о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬�����¶Ȳ�ͬ������������ȫ��ͬ��
��2����������Һ�в����Ũ�ȣ�Ȼ�����v=$\frac{��c}{��t}$�������ʱ����ڲ����ƽ����Ӧ���ʣ�
��3����Ӧ�ų�����=�������γ��¼��ų���������-��Ӧ����Ѿɼ����յ����������ݴ˽��м��㣻
��4�����淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�����ֵ�Ũ�ȡ��ٷֺ������ٱ仯���ݴ˽����жϣ�
��� �⣺��1������о������Ի�ѧ��Ӧ���ʵ�Ӱ�죬Ӧ�ó��˴�����ͬ������������ȫ��ͬ�����ݱ������ݿ�֪���٢����¶ȡ�����������ȫ��ͬ��Ӧ����̽�������Է�Ӧ���ʵ�Ӱ�죻ʵ��ٺ͢��г����¶Ȳ�ͬ�⣬����������ȫ��ͬ����̽�������¶ȶԷ�Ӧ���ʵ�Ӱ�죬
�ʴ�Ϊ���٣��ڣ��٣��ۣ�
��2������5���ӷ�Ӧ��ʵ����в�����ȫ���ģ����Һ�в���Ũ��Ϊ��$\frac{0.5mol/L��0.002L}{0.004L+0.002L+0.002L}$=0.125mol/L��������ƽ����Ӧ����Ϊ��$\frac{0.125mol/L}{5min}$=0.025mol/��L•min����
�ʴ�Ϊ��0.025mol/��L•min����
��3����Ӧ���ɵ�CO2���������ϳɼ״���CH3OH����CO2��g��+3H2��g���TCH3OH��g��+H2O��g�����÷�Ӧ�Ƿ��ȷ�Ӧ������1mol CO2�еĻ�ѧ����������Q1kJ������1mol H2�еĻ�ѧ����������Q2kJ���γ�1mol CH3OH�еĻ�ѧ���ͷ�����Q3kJ���γ�1mol H2O�еĻ�ѧ���ͷ�����Q4kJ����������£�����1mol CH3OH�ų�������=�������γ��¼��ų���������-��Ӧ����Ѿɼ����յ�������=3Q3kJ+Q4kJ-3Q2kJ-Q1kJ=��3Q3+Q4-3Q2-Q1��kJ��
�ʴ�Ϊ����3Q3+Q4-3Q2-Q1��kJ��
��4��A���ﵽƽ��״̬ʱ������ֵ�Ũ�Ȳ��ٱ仯���������ʵ�Ũ�Ȳ�һ����ȣ���A����
B���ÿ��淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�������3mol H2����ͬʱ����1mol CH3OH����B��ȷ��
C�������¶Ⱥ����淴Ӧ���ʶ������÷�Ӧ�Ƿ��ȷ�Ӧ����ƽ�����������ƶ�����C����
�ʴ�Ϊ��B��
���� ���⿼����Ӱ�컯ѧ��Ӧ���ʵ����ء��Ȼ�ѧ����ʽ�ļ��㡢��ѧƽ��״̬���жϵ�֪ʶ����Ŀ�Ѷ��еȣ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ�����������������ѧʵ�顢��ѧ����������

 ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�| A�� | ��ͬ�Ļ�ѧ��Ӧ���ȿ��ܲ�ͬ | |
| B�� | ����ͨ���ı䷴Ӧ��Ũ�������ƻ�ѧ��Ӧ���� | |
| C�� | ����ͨ���ӳ���ѧ��Ӧ��ʱ�����ı䷴Ӧ���� | |
| D�� | �������ܿ��ƻ�ѧ��Ӧ���� |
| A�� | ��ϩ���廯�����������뱽���巴Ӧ���屽 | |
| B�� | ������ˮ�����ɰ���������۷������ɾƾ� | |
| C�� | �Ҵ���ˮ����ϩ���Ҵ���������ˮ���������� | |
| D�� | �����������һ�ȼ����뱽�����ᷴӦ�������� |
| A�� | CH4+3Cl2$\stackrel{����}{��}$CHCl3+3HCl��ȡ����Ӧ�� | |
| B�� | nH2C=CHCl��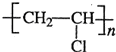 �����۷�Ӧ�� �����۷�Ӧ�� | |
| C�� | 2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��������Ӧ�� | |
| D�� | CH3COOH+CH3OH$��_{��}^{Ũ����}$CH3COOCH3+H2O����ȥ��Ӧ�� |
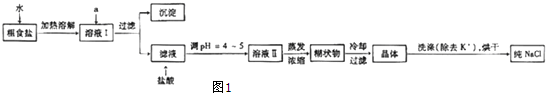
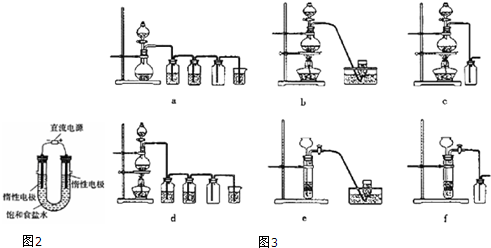
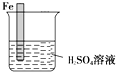 ���������dz�����ԭ���װ�öԽ������з�������������ͼ1�Ļ��������һ��ԭ���װ�ã���ֹ����һ�������ᷴӦ��
���������dz�����ԭ���װ�öԽ������з�������������ͼ1�Ļ��������һ��ԭ���װ�ã���ֹ����һ�������ᷴӦ��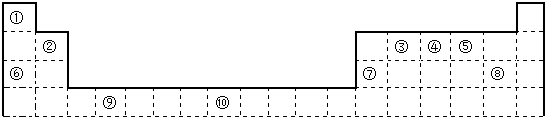
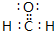 �����ݼ۲���ӶԻ��⣨VSEPR�������Ʋ�÷��ӵĿռ乹��Ϊƽ�������Σ�
�����ݼ۲���ӶԻ��⣨VSEPR�������Ʋ�÷��ӵĿռ乹��Ϊƽ�������Σ�