题目内容
【题目】(1)下列元素或化合物的性质变化顺序正确的是__________________
A.第一电离能:Cl>S>P>Si
B.共价键的极性:HF>HCl>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI
D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
(2)FeCl3 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的 FeCl3 的结构式为_________,其中 Fe 的配位数为___________________
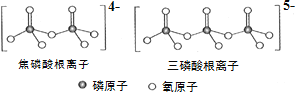
(3)NH4H2PO4 中,电负性最高的元素是________;P的________________杂化轨道与 O的2p轨道形成______键。NH4H2PO4 和 LiFePO4 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐, 如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示。这类磷酸根离子的化学式可用通式表示为 ______________(用 n 代表 P 原子数)。
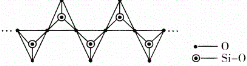
(4)高温高压下 CO2 的晶体结构与SiO2 相似,该晶体熔点比 SiO2 晶体____________(填“高”或“低”)。硅酸盐和 SiO2 一样,都是以硅氧四面体作为基本结构单元,图中表示一种含 n 个硅原子的单链式多硅酸根的结构(投影如图),Si 原子的杂化类型为_______________,其化学通式可表示为____________________
(5)四方晶系 CuFeS2 晶胞结构如图所示(下一页)。Cu2+的配位数为_______________,S2-的配位数为__已知:a=b=0.524 nm,c=1.032 nm,NA 为阿伏加德罗常数的值,CuFeS2晶体的密度是_________________ gcm-3(列出计算式)。

【答案】BC ![]() 4 O sp3 σ (PnO3n+1)(n+2)- 高 sp3 (SiO3)n 2n- 4 4
4 O sp3 σ (PnO3n+1)(n+2)- 高 sp3 (SiO3)n 2n- 4 4 ![]()
【解析】
(1)A.第一电离能,一般与非金属性成正比,当电子亚层处于半满、全满时出现反常;
B.对于氢化物分子,非金属性越强,键的极性越强;
C.晶格能与离子的带电荷成正比,与离子半径的平方成反比;
D.热稳定性与分解产物的稳定性有关。
(2)蒸汽状态下以双聚分子存在的 FeCl3 的结构式与Al2Cl6类似,由结构可确定 Fe 的配位数。
(3)NH4H2PO4 中,电负性最高的元素也就是非金属性最强的元素;P与周围的4个O原子相连,价层电子对数为4,从而确定与 O的2p轨道形成的键型。由两个已知结构式寻找规律,得出图中磷酸根离子的化学式通式。
(4)比较原子晶体熔点,可比较原子半径,半径越小,熔点越高。图中表示一种含 n 个硅原子的单链式多硅酸根的结构,Si 原子的价层电子对数为4,由此确定杂化类型,确定化学通式时,可采用均摊法。
(5)Cu2+位于面心,有2个S2-与它相连;1个S2-与2个Cu2+、2个Fe2+相连。已知:a=b=0.524 nm,c=1.032 nm,可求出体积,NA 为阿伏加德罗常数的值,求CuFeS2晶体的密度,只需求出1个晶胞中所含离子的数目。
(1)A.由于P原子的3p轨道半充满,第一电离能出现反常,所以第一电离能:Cl>P>S>Si,A不正确;
B.对于氢化物分子,非金属性越强,键的极性越强,所以共价键的极性:HF>HCl>HBr>HI,B正确;
C.晶格能与离子的带电荷成正比,与离子半径的平方成反比,所以晶格能:NaF>NaCl>NaBr>NaI,C正确;
D.对于同主族元素的碳酸盐,金属性越强,其氧化物越稳定,碳酸盐的热稳定性越差,所以热稳定性:MgCO3<CaCO3<SrCO3<BaCO3,D不正确;
故选BC。答案为:BC;
(2)FeCl3蒸汽状态下以双聚分子存在,则类似于Al2Cl6,即每个Fe与4个Cl形成共价键,其中有1个是配位键,从而得出FeCl3 的结构式为![]() ,其中 Fe 的配位数为4。答案为:
,其中 Fe 的配位数为4。答案为:![]() ;4;
;4;
(3)NH4H2PO4 中,电负性最高的元素是O;P与周围的4个O原子相连,价层电子对数为4,所以P的sp3杂化轨道与 O的2p轨道形成σ键。分析磷酸根离子中P、O原子个数的递变规律,可得出其化学式可用通式表示为(PnO3n+1)(n+2)-。答案为:O;sp3;σ;(PnO3n+1)(n+2)-;
(4)高温高压下 CO2 的晶体结构与SiO2 相似,也为原子晶体。比较原子晶体熔点时,可比较原子半径,半径越小,熔点越高,所以该晶体熔点比 SiO2 晶体高。从一种含 n 个硅原子的单链式多硅酸根的结构图中可以看出,每个Si与4个O相连,所以Si 原子的杂化类型为sp3,在每个结构单元中,有1个Si、4个O,其中有2个O完全属于此结构单元,有2个O被两个结构单元共用,从而得出其化学通式可表示为(SiO3)n 2n-。答案为:高;sp3;(SiO3)n 2n-;
(5)由晶胞结构分析可知,面心上的Cu2+与2个S2-相连,晶胞中每个Cu2+与4个S2-相连,Cu2+的配位数为4;1个S2-与2个Cu2+、2个Fe2+相连,则每个S2-的配位数为4。晶胞中,Fe2+数为8×![]() +4×
+4×![]() +1=4,Cu2+数为6×
+1=4,Cu2+数为6×![]() +4×
+4×![]() =4,S2-数为8,晶胞内共含4个CuFeS2,a=b=0.524 nm,c=1.032 nm,NA 为阿伏加德罗常数的值,CuFeS2晶体的密度是
=4,S2-数为8,晶胞内共含4个CuFeS2,a=b=0.524 nm,c=1.032 nm,NA 为阿伏加德罗常数的值,CuFeS2晶体的密度是![]() gcm-3。答案为:4;4;
gcm-3。答案为:4;4;![]() 。
。

 灵星计算小达人系列答案
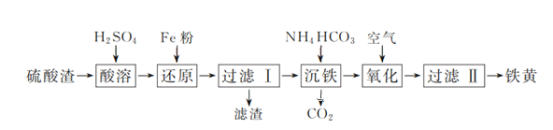
灵星计算小达人系列答案【题目】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备CuSO4·5H2O,主要步骤如下:
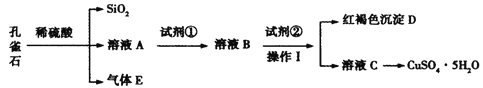
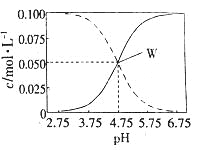
已知该条件下,通过调节溶液的酸碱性而使 Fe3+、Fe2+、Cu2+生成沉淀的 pH 分别如下:
物质 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe(OH)3 | 2.2 | 3.2 |
Fe(OH)2 | 7.6 | 9.6 |
Cu(OH)2 | 4.7 | 6.4 |
请回答下列问题:
(1)为了提高孔雀石酸浸时的速率,除适当增加浓硫酸浓度外,还可以采取的措施有:___(写一种)。
(2)试剂①是双氧水,把 Fe2+氧化成 Fe3+的目的是___。根据如图有关数据,你认为工业上氧化操作时应采取的条件是___。

(3)试剂②为CuO,其目的是调节溶液的 pH 保持在___范围。操作Ⅰ的名称是___。
(4)溶液 C 得到CuSO4·5H2O的主要步骤是___、___、过滤、洗涤、干燥。
【题目】(一)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
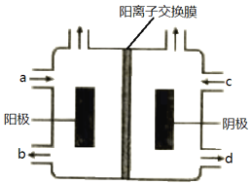
(1)收集到(CH3)4NOH的区域是________(填a、b、c或d)。
(2)写出电池总反应_____________。
(二)乙酸乙酯一般通过乙酸和乙醇酯化合成:CH3COOH(l)+C2H5OH(l) ![]() CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
已知纯物质和相关恒沸混合物的常压沸点如下表:
纯物质 | 沸点/℃ | 恒沸混合物(质量分数) | 沸点/℃ |
乙醇 | 78.3 | 乙酸乙酯(0.92)+水(0.08) | 70.4 |
乙酸 | 117.9 | 乙酸乙酯(0.69)+乙醇(0.31) | 71.8 |
乙酸乙酯 | 77.1 | 乙酸乙酯(0.83)+乙醇(0.08) +水(0.09) | 70.2 |
请完成:
(1)关于该反应,下列说法不合理的是_____________。
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
(2)一定温度下该反应的平衡常数K=4.0。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y =_________;若乙酸和乙醇的物质的量之比为n : 1,相应平衡体系中乙酸乙酯的物质的量分数为x,请在图中绘制x随n变化的示意图(计算时不计副反应)________。

(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有___________________。
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g) ![]() CH3COOC2H5(g)+2H2(g)
CH3COOC2H5(g)+2H2(g)
在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是_____。

A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键