��Ŀ����
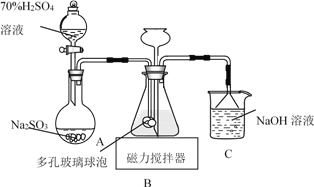
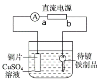
����Ŀ��ij��ѧ��ȤС�������ͼ��ʾװ�ã���CuCl2��2H2O�����SOCl2��ȡ��ˮCuCl2�����չ�����SOCl2��

��֪��SOCl2���۵�Ϊ��105�棬�е�Ϊ76�棬��ˮ���ҷ�Ӧ���������������塣
�ش��������⣺
��1��CuCl2��2H2O�����SOCl2������Ӧ�Ļ�ѧ����ʽ��___��
��2����ʯ�ҳ���������SO2��HCl���������壬����������Ϊ__��
��3��ijͬѧ������ӵ��������ⶨ��ˮCuCl2��Ʒ��ͭԪ�صİٷֺ����������������£�
����1��ȡ0.2500g��������ˮ���������KI�����ַ�Ӧ�����ɰ�ɫCuI������
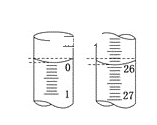
����2�����뼸�ε�����Һ��
����3���ٵ���0.1000mol��L-1Na2S2O3��Һ�������ķ�ӦΪ2S2O32-��I2=S4O62-��2I-��ǡ����ȫ��Ӧʱ������Na2S2O3��Һ18.00mL��
��ǡ����ȫ��Ӧʱ��ʵ������Ϊ__��
�ڼ���������ͭԪ�ص���������__(д���������)��
���𰸡�CuCl2��2H2O��2SOCl2=CuCl2��2SO2����4HCl�� ��ֹ������ˮ����������ƿ����SOCl2������Ӧ ��Һ����ɫ��Ϊ��ɫ 46.1%
��������
��SOCl2Һ����뵽CuCl2��2H2O�����У�������Ӧ����CuCl2���������SOCl2�����ȥ��������������ƿ�н��ܣ�ע���ֹSOCl2��ˮ���ҷ�Ӧ�����Ҫ�ü�ʯ�ҷ�ֹ������ˮ�������뵽��ƿ�С�
��SOCl2��ˮ���ҷ�Ӧ���������������壬���CuCl2��2H2O�����SOCl2������Ӧ�Ļ�ѧ����ʽ��CuCl2��2H2O��2SOCl2=CuCl2��2SO2����4HCl�����ʴ�Ϊ��CuCl2��2H2O��2SOCl2 = CuCl2��2SO2����4HCl����
�Ƽ�ʯ�ҳ���������SO2��HCl���������壬����SOCl2��ˮ���ҷ�Ӧ����˼�ʯ�һ���������Ϊ��ֹ������ˮ����������ƿ����SOCl2������Ӧ���ʴ�Ϊ����ֹ������ˮ����������ƿ����SOCl2������Ӧ��
������ʼ�еⵥ�ʣ���������Ӧ�꣬���ǡ����ȫ��Ӧʱ��ʵ������Ϊ��Һ����ɫ��Ϊ��ɫ���ʴ�Ϊ����Һ����ɫ��Ϊ��ɫ��
�����ݷ�Ӧ����ʽ�õ���ϵʽ2Cu2+ �� I2 �� 2S2O32��n(Na2S2O3) = n(Cu2+) = 0.1000mol��L1��0.018L = 0.0018mol��![]() ���ʴ�Ϊ46.1%��
���ʴ�Ϊ46.1%��

 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д� С����ȫ�ܼ��ϵ�д�
С����ȫ�ܼ��ϵ�д�