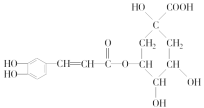
题目内容
【题目】实验室制取溴乙烷的主反应如下:

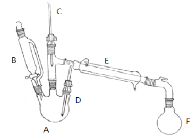
副反应:在该实验中经常会有乙醚、溴等副产物生成,装置如图所示。
相对分子质量 | 密度/(g·cm—3) | 沸点/℃ | 溶解度 | |
乙 醇 | 46 | 0.789 | 78.3 | 易溶 |
溴乙烷 | 109 | 1.46 | 38.2 | 难溶 |
浓硫酸 | 98 | 1.84 | 338.0 | 易溶 |
实验步骤:
①向A中先加入5 mL 95%的无水乙醇(0.085 mol)和4.5 mL的水,加入溴化钠7.725 g ,再加入沸石,摇匀。在接受器F中加冷水及3ml饱和亚硫酸氢钠溶液,并将其放入冰水浴中。
②在B中加入9.5 mL浓硫酸(0.17 mol),向A中缓缓滴入浓硫酸,加热体系,控制反应温度,保持反应平稳地发生,直至无油状物馏出为止;
③分出馏出液中的有机层,加入1-2 mL浓硫酸以除去乙醚、乙醇、水等杂质,溶液明显分层后,分离得到粗产物;
④将粗产物转入蒸馏瓶中,加入沸石,在水浴上加热蒸馏,收集35-40℃的馏分,称量得5.23g。
回答问题:
(1)仪器E的名称为 ;反应装置中有使用C、D两根温度计,其中D温度计的作用是: 。
(2)步骤①在接受器F中加冷水以及将F放入冰水浴中的目的是 。饱和亚硫酸氢钠溶液的作用是 ;
(3)步骤②中浓硫酸要缓缓滴加而不一次加入,其作用有 (填标号)。
A.可以防止乙醇发生碳化 b.避免生成HBr的速度过快,减少其挥发
c.避免溶液发生暴沸 D.减少因浓硫酸氧化HBr而生成副产物溴;
(4)步骤③中分出馏出液中有机层的操作名称为 。加入浓硫酸除杂后的溶液明显分层,粗产物在 层(填“上”或“下”);
(5)本实验的产率为 。
【答案】(1)冷凝管(2分);D温度计用来测反应体系的温度(2分)
(2)溴乙烷沸点低、极易挥发,冰水主要可以防止溴乙烷的挥发(2分)除去反应中的副产物溴(2分)
(3)abd (2分) (4)分液(1分) 上(1分) (5)64%(3分)
【解析】
试题分析:(1)根据仪器的构造可判断仪器E的名称为冷凝管;反应装置中D温度计水银球插入反应液中,因此其作用是用来测反应体系的温度。
(2)由于溴乙烷沸点低、极易挥发,冰水主要可以防止溴乙烷的挥发,因此步骤①在接受器F中加冷水以及将F放入冰水浴中。溴易挥发且有毒,因此饱和亚硫酸氢钠溶液的作用是除去反应中的副产物溴;
(3)步骤②中浓硫酸要缓缓滴加而不一次加入,其作用有 (填标号)。
A.浓硫酸具有脱水性,缓缓加入浓硫酸可以防止乙醇发生碳化,a正确;B.浓硫酸与溴化钠反应生成溴化氢,缓缓加入浓硫酸可以避免生成HBr的速度过快,减少其挥发,b正确;C.溶液发生暴沸与反应体系的温度有关系,c错误;D.浓硫酸具有强氧化性,能氧化溴化氢,因此缓缓加入可减少因浓硫酸氧化HBr而生成副产物溴,d正确,答案选abd。
(4)溴乙烷不溶于水,因此步骤③中分出馏出液中有机层的操作名称为分液。由于溴乙烷的密度小于浓硫酸的,因此加入浓硫酸除杂后的溶液明显分层,粗产物在上层;
(5)7.725 g溴化钠的物质的量是7.725g÷103g/mol=0.075mol,产生溴化氢0.075mol,乙醇是0.085mol,因此生成的溴乙烷按照溴化氢的物质的量计算,即产生溴乙烷是0.075mol,理论上得到溴乙烷的质量是0.075mol×109g/mol=8.175g,所以本实验的产率为![]() 。
。

【题目】己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如图表: ![]()
物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 |
环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |

实验步骤如下:
Ⅰ.在三口烧瓶中加入16mL 50%的硝酸(密度为l.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80℃一90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
V.粗产品经提纯后称重为5.7g
请回答下列问题:
(1)本实验所用50%的HNO3溶液物质的量浓度为 (保留一位小数),滴液漏斗中的细支管a作用是 。
(2)仪器b的名称为 ,其作用是 ,使用时要从 (填“上口”或“下口”)通入冷水。
(3)NaOH溶液的作用是 。溶液上方倒扣的漏斗的作用是 。
(4)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(5)为了除去可能的杂质和减少产品损失,可分别用 和 洗涤晶体。