��Ŀ����
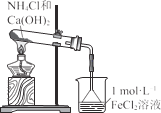
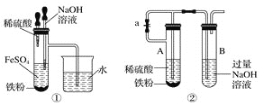
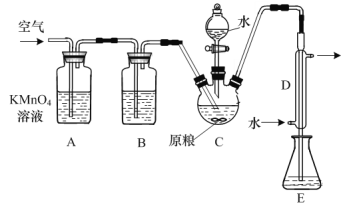
����Ŀ����ʳ�ִ���������(AlP)Ѭ��ɱ�棬AlP��ˮ������ǿ��ԭ�Ե�PH3���塣���ұ��涨��ʳ������(��PH3��)�IJ�����������0.05mg��kg-1Ϊ�ϸ�ijС��ͬѧ����ͼ��ʾʵ��װ�ú�ԭ���ⶨij��ʳ��Ʒ������IJ�������C�м���100gԭ����E�м���20.00mL 2.50��10-4mol��L-1 KMnO4��Һ(H2SO4�ữ)����C�м�������ˮ����ַ�Ӧ�����������Ʊ���Һ�ζ�E�е���Һ��
��1����Ӧ�����ͨ�������������_______��
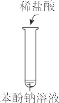
��2��װ��B��ʢװ����ûʳ����ļ�����Һ�������������տ����е�_______���ѧʽ����
��3��װ��E��PH3�����������ᣬMnO![]() ����ԭΪMn2������PH3��MnO
����ԭΪMn2������PH3��MnO![]() ��Ӧ�����ʵ���֮��Ϊ_______��
��Ӧ�����ʵ���֮��Ϊ_______��
��4���ռ�װ��E�е�����Һ����ˮϡ����250mL����ȡ���е�25.00mL����ƿ�У���6.0��10-5mol��L-1��Na2SO3����Һ�ζ�������Na2SO3����Һ20.00 mL����Ӧԭ���ǣ�SO![]() ��MnO
��MnO![]() ��H+= SO
��H+= SO![]() ��Mn2+��H2O(δ��ƽ)��ͨ�������жϸ���Ʒ�Ƿ�ϸ�(д���������)_____��
��Mn2+��H2O(δ��ƽ)��ͨ�������жϸ���Ʒ�Ƿ�ϸ�(д���������)_____��
���𰸡��ž�װ��C�в�����PH3���壬ʹPH3��E��KMnO4��Һ��ȫ���� O2 5��8 25 mL����Һ�в�����KMnO4��
n(KMnO4������)��![]() ��6.0��10-5 mol��L-1��20��10-3L��4.8��10-7 mol
��6.0��10-5 mol��L-1��20��10-3L��4.8��10-7 mol
250 mL����Һ�з�Ӧ��KMnO4��
n(KMnO4����Ӧ)=2.50��10-4mol��L-1��20��10-3L��4.8��10-7mol��![]()
��2��10-7mol
n(PH3)��2��10-7mol ��![]() ��1.25��10-7mol
��1.25��10-7mol
m(PH3)��1.25��10-7mol��34 g��mol-1��4. 25��10-6g
����IJ������� ![]() ��0.0425mg��kg-1��0.05mg��kg-1�����Ժϸ�
��0.0425mg��kg-1��0.05mg��kg-1�����Ժϸ�
��������
C��ʢ��100gԭ����E��ʢ��20.00mL 2.50��10-4 mol/L��KMnO4��Һ��H2SO4�ữ�����������ɵ�PH3��B��ʢװ����ûʳ����ļ�����Һ�������������տ����е�O2����ֹ����װ��C�����ɵ�PH3��A��ʢװKMnO4��Һ�����ó�ȥ�����еĻ�ԭ�����壻
��1��ͨ����������ɵ�PH3ȫ��������������Һ�����գ���Ӧ�����ͨ��������������ž�װ��C�в�����PH3���壬ʹPH3��E��KMnO4��Һ��ȫ���գ�
��2������������PH3�����Ӧ��ȥ������
��3��װ��E��PH3�����������ᣬ���������Һ����ԭ���������ӣ�ͬʱ����ˮ���ɣ�
��4��E��ʢ��20.00mL 2.50��10-4 mol/L��KMnO4��Һ��H2SO4�ữ���������������ɵ�PH3��������Ӧ��5PH3+8MnO![]() +24H+=5H3PO4+8Mn2++12H2O��Na2SO3����Һ�ζ�ʣ���KMnO4��Һ�����÷���ʽ5SO
+24H+=5H3PO4+8Mn2++12H2O��Na2SO3����Һ�ζ�ʣ���KMnO4��Һ�����÷���ʽ5SO![]() +2MnO
+2MnO![]() +6H+=5 SO
+6H+=5 SO![]() +2Mn2++3H2O����ʣ���KMnO4�����ʵ���������������PH3��Ӧ��KMnO4�����ʵ��������б�������PH3�����ʵ�������������PH3�IJ�������
+2Mn2++3H2O����ʣ���KMnO4�����ʵ���������������PH3��Ӧ��KMnO4�����ʵ��������б�������PH3�����ʵ�������������PH3�IJ�������
��1��ͨ����������ɵ�PH3ȫ��������������Һ�����գ���Ӧ�����ͨ��������������ž�װ��C�в�����PH3���壬ʹPH3��E��KMnO4��Һ��ȫ���գ�
��2��B��ʢװ����ûʳ����ļ�����Һ�������������տ����е�O2����ֹ����װ��C�����ɵ�PH3��
��3��װ��E��PH3�����������ᣬMnO![]() ����ԭΪMn2����ͬʱ����ˮ���ɣ����ݵ�ʧ�����غ㡢����غ㡢Ԫ���غ�д���÷�Ӧ�����ӷ���ʽΪ��5PH3+8MnO
����ԭΪMn2����ͬʱ����ˮ���ɣ����ݵ�ʧ�����غ㡢����غ㡢Ԫ���غ�д���÷�Ӧ�����ӷ���ʽΪ��5PH3+8MnO![]() +24H+=5H3PO4+8Mn
+24H+=5H3PO4+8Mn![]() ��Ӧ�����ʵ���֮��Ϊ5��8��
��Ӧ�����ʵ���֮��Ϊ5��8��
��4��25 mL����Һ�в�����KMnO4��
n(KMnO4������)=![]() ��6.0��10-5mol��L-1��20��10-3L=4.8��10-7mol
��6.0��10-5mol��L-1��20��10-3L=4.8��10-7mol
250 mL����Һ�з�Ӧ��KMnO4��
n(KMnO4����Ӧ)��2.50��10-4mol��L-1��20��10-3L��4.8��10-7mol��![]() =2��10-7mol
=2��10-7mol
n(PH3)=2��10-7mol ��![]() =1.25��10-7mol
=1.25��10-7mol
m(PH3)=1.25��10��7mol��34g��mol-1=4. 25��10-6g
����IJ������� ![]() =0.0425mg��kg-1��0.05mg��kg-1�����Ժϸ�
=0.0425mg��kg-1��0.05mg��kg-1�����Ժϸ�
n(KMnO4������)=![]() ��6.0��10-5 mol��L-1��20��10-3L=4.8��10-7 mol
��6.0��10-5 mol��L-1��20��10-3L=4.8��10-7 mol
250 mL����Һ�з�Ӧ��KMnO4��
n(KMnO4����Ӧ)=2.50��10-4mol��L-1��20��10-3L-4.8��10-7mol��![]() =2��10-7mol
=2��10-7mol
n(PH3)=2��10-7 mol ��![]() =1.25��10-7 mol
=1.25��10-7 mol
m(PH3)=1.25��10��7 mol��34 g��mol-1=4. 25��10��6 g
����IJ�������![]() =0.0425 mg��kg-1��0.05 mg��kg-1�����Ժϸ�
=0.0425 mg��kg-1��0.05 mg��kg-1�����Ժϸ�

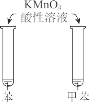
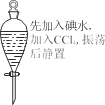
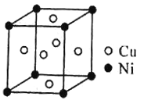
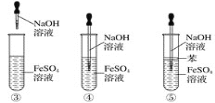
����Ŀ������ʵ������Ԥ����ȷ����
A | B | C | D |
|
|
|
|
�ձ��в�����ɫ������һ��ʱ�����������Ա仯 | ��������ְ�ɫ���ǣ����ȱ���� | KMnO4 ������Һ�ڱ��ͼױ��о���ɫ | Һ��ֲ㣬�²�� ��ɫ |
A.AB.BC.CD.D
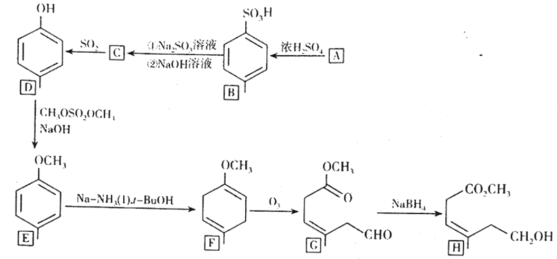
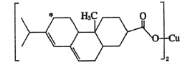
����Ŀ����ҵ�Ͽ���![]() ��
��![]() �ϳ���������
�ϳ���������![]() �����������л��ϳɡ��ش��������⣺
�����������л��ϳɡ��ش��������⣺
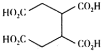
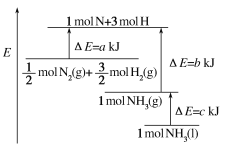
(1)һ�������£����������������ڴ����еĺ������������ʱ�������������ȣ��漰�йط�Ӧ���Ȼ�ѧ����ʽ���£�
��![]()
��![]()
��![]()
��![]()
![]() __________(��
__________(��![]() ��
��![]() ��ʾ)��
��ʾ)��
(2)![]() ʱ����һ�ܱ������з�����Ӧ��
ʱ����һ�ܱ������з�����Ӧ��![]() ��������Ӧ���ʱ���ʽ
��������Ӧ���ʱ���ʽ![]() ���������Ӧ���ʺͶ�ӦŨ�ȵ����������
���������Ӧ���ʺͶ�ӦŨ�ȵ����������
��� |
|
|
�� |
|
|
�� |
|
|
�� |
|
|
��![]() __________�ﵽƽ�������Сѹǿ�����������ƽ����Է���������__________(ѡ����������������С������������)��
__________�ﵽƽ�������Сѹǿ�����������ƽ����Է���������__________(ѡ����������������С������������)��
(3)![]() ʱ�������Ϊ
ʱ�������Ϊ![]() �Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��
�Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��![]() ��
��![]() ������Ӧ��
������Ӧ��
![]() ����֪����Ӧ��ʼ��ƽ��ʱ�¶���ͬ��
����֪����Ӧ��ʼ��ƽ��ʱ�¶���ͬ��

�ٲ�÷�Ӧ������ѹǿ![]() ��ʱ��
��ʱ��![]() �ı仯��ͼ1����
�ı仯��ͼ1����![]() ��ʾ����
��ʾ����![]() __________(ѡ����>������<��������ȷ����)0��������������ͬ�����ı�ijһ����ʱ�����ѹǿ
__________(ѡ����>������<��������ȷ����)0��������������ͬ�����ı�ijһ����ʱ�����ѹǿ![]() ��ʱ��
��ʱ��![]() �ı仯��ͼ1����
�ı仯��ͼ1����![]() ��ʾ����ı��������_________��
��ʾ����ı��������_________��
��ͼ2����λͬѧ����������Ӧƽ�ⳣ���Ķ���ֵ![]() ���¶ȵı仯��ϵͼ��������ȷ��������______(ѡ����������������)��
���¶ȵı仯��ϵͼ��������ȷ��������______(ѡ����������������)��![]() ��ֵΪ______��
��ֵΪ______��