题目内容
6.下列说法错误的是( )| A. | 鸡蛋清和淀粉可以用浓硝酸鉴别 | |
| B. | 用甘氨酸和丙氨酸缩合最多可形成4种二肽 | |
| C. | 分子式为C5H8O2,既与碳酸钠溶液反应又与溴的四氯化碳溶液反应的有机物有8种 | |
| D. | 乳酸薄荷醇酯(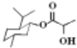 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 |
分析 A.蛋白质可与浓硝酸发生颜色反应;
B.氨基酸形成肽键原理为羧基提供-OH,氨基提供-H,两个氨基酸分子脱去一个水分子脱水结合形成二肽,既要考虑不同氨基酸分子间生成二肽,又要考虑同种氨基酸分子间形成二肽;
C.能与Na2CO3,溶液反应生成CO2,说明此分子含有羧基,能与溴的四氯化碳溶液反应说明此分子含有碳碳双键,然后根据官能团的位置异构和碳链异构确定;
D.含-COOC-可发生水解,含-OH可发生取代、氧化、消去反应.
解答 解:A.鸡蛋清的主要成分为蛋白质,蛋白质可与浓硝酸发生颜色反应,可鉴别,故A正确;
B.氨基酸生成二肽,就是两个氨基酸分子脱去一个水分子.当同种氨基酸脱水,生成2种二肽;当是异种氨基酸脱水:可以是甘氨酸脱去羟基,丙氨酸脱氢;也可以丙氨酸脱羟基,甘氨酸脱去氢,生成2种二肽,共4种,故B正确;
C.能与Na2CO3,溶液反应生成CO2,说明此分子含有羧基,能与溴的四氯化碳溶液反应说明此分子含有碳碳双键,根据碳链异构和双键、羧基官能团异构可得8种同分异构体,分别为: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 ,故C正确;
,故C正确;
D. 分子中含-COOC-可发生水解反应,含-OH可发生氧化反应、消去反应,羟基还可发生取代反应,故D错误;
分子中含-COOC-可发生水解反应,含-OH可发生氧化反应、消去反应,羟基还可发生取代反应,故D错误;
故选D.
点评 本题考查了有机物结构与性质,题目难度中等,注意掌握常见有机物结构与性质,明确酯化反应原理,C为难点、易错点,注意掌握同分异构体的概念及书写原则,避免重复或遗漏现象.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列反应的离子方程式书写不正确的是( )
| A. | Ba(OH)2溶液与CuSO4溶液反应:Ba2++SO42-=BaSO4↓ | |
| B. | NaOH溶液与稀硫酸的反应:OH-+H+=H2O | |
| C. | NaHCO3溶液与盐酸的反应:HCO3-+H+=H2O+CO2↑ | |
| D. | KCl溶液与AgNO3溶液的反应:Cl-+Ag+=AgCl↓ |
1.元素A的单质及A与B形成的化合物能按如图所示的关系发生转化.则下列说法正确的是( )
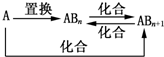

| A. | 图中物质间的转化都不是氧化还原反应 | |
| B. | 当n=1时,A可能是N2 | |
| C. | A一定是金属元素 | |
| D. | 当n=2时,A可能是Fe |
11.下列排列顺序正确的是( )
| A. | 原子序数:C>Li>B | B. | 元素的非金属性:N>O>F | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 氢化物的稳定性:HF>HCl>HBr |
18.已知反应:
①101KPa时,2C(s)+O2(g)=2CO(g);△H=-221KJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3KJ/mol
下列结论正确的是( )
①101KPa时,2C(s)+O2(g)=2CO(g);△H=-221KJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3KJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热等于110.5KJ/mol | |
| B. | 2C(s)+2O2(g)=2CO2(g);△H>-221 KJ/mol | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热为-57.3 KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出热量小于57.3 KJ |
15.一定温度下,在一固定体积的密闭容器中,可逆反应A(s)+3B(g)?2C(g)达到平衡时,下列说法正确的是( )
①C的生成速率和C的分解速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化 ④混合气体的总压强不再变化 ⑤A、B、C物质的量之比为1:3:2
⑥混合气体的平均相对分子质量不变 ⑦容器中C的体积分数不变.
①C的生成速率和C的分解速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化 ④混合气体的总压强不再变化 ⑤A、B、C物质的量之比为1:3:2
⑥混合气体的平均相对分子质量不变 ⑦容器中C的体积分数不变.
| A. | ②④⑤⑦ | B. | ①③④⑥⑦ | C. | ①④⑥⑦ | D. | ①③④⑤ |
16.下列各组离子,一定能在指定环境中大量共存的是( )
| A. | pH=0的溶液中:K+、ClO-、CH3CHO、SO42- | |
| B. | c(H+)=10-12mol•L-1的溶液中:Na+、NH4+、Cl-、Br- | |
| C. | 加人KSCN显血红色的溶液中:Br-、NO3-、SO42-、Mg2+ | |
| D. | 在加入Al能放出大量H2的溶液中:NH4+、SO42-、C1-、HCO3- |