题目内容
16.下列各组离子,一定能在指定环境中大量共存的是( )| A. | pH=0的溶液中:K+、ClO-、CH3CHO、SO42- | |
| B. | c(H+)=10-12mol•L-1的溶液中:Na+、NH4+、Cl-、Br- | |
| C. | 加人KSCN显血红色的溶液中:Br-、NO3-、SO42-、Mg2+ | |
| D. | 在加入Al能放出大量H2的溶液中:NH4+、SO42-、C1-、HCO3- |
分析 A.pH=0的溶液为酸性溶液,溶液中存在大量氢离子,次氯酸根离子与氢离子反应生成次氯酸,次氯酸能够氧化乙醛;
B.c(H+)=10-12mol•L-1的溶液为碱性溶液,溶液中存在大量氢氧根离子,铵根离子与氢氧根离子反应;
C.加人KSCN显血红色的溶液中存在大量铁离子,四种离子之间不反应,都不与铁离子反应;
D.加入Al能放出大量H2的溶液中存在大量氢离子或氢氧根离子,铵根离子、碳酸氢根离子与氢氧根离子反应,碳酸氢根离子还能够与氢离子反应.
解答 解:A.pH=0的溶液中存在大量氢离子,ClO-与氢离子结合生成次氯酸,次氯酸能够氧化CH3CHO,在溶液中不能大量共存,故A错误;
B.c(H+)=10-12mol•L-1的溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.加人KSCN显血红色的溶液中存在大量Fe3+,Br-、NO3-、SO42-、Mg2+之间不发生反应,都不与Fe3+反应,在溶液中能够大量共存,故C正确;
D.加入Al能放出大量H2的溶液为酸性或强碱性溶液,溶液中存在大量氢离子或氢氧根离子,NH4+与氢氧根离子反应,HCO3-既能够与氢离子,也能够与氢氧根离子反应,在溶液中一定不能大量共存,故D错误;
故选C.
点评 本题考查了离子共存,题目难度中等,明确题干暗含条件的含义为解答关键,注意熟练掌握常见离子的性质及离子反应发生条件,合理把握离子之间能够共存的情况,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列说法错误的是( )
| A. | 鸡蛋清和淀粉可以用浓硝酸鉴别 | |
| B. | 用甘氨酸和丙氨酸缩合最多可形成4种二肽 | |
| C. | 分子式为C5H8O2,既与碳酸钠溶液反应又与溴的四氯化碳溶液反应的有机物有8种 | |
| D. | 乳酸薄荷醇酯(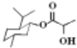 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 |
11.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | HBrO4的酸性比HClO4的酸性强 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | 硒化氢(H2Se)是无色、有毒且无硫化氢稳定的气体 |
1.某无色溶液中可能含有H+、OH-、K+、NO3-,加入铝粉后,只产生H2.试回答:
(1)加入铝粉产生H2,说明铝具有还原性(填“氧化性”或“还原性”).
(2)甲同学分析:若H+大量存在,则NO3-就不能大量存在.设计实验证实如表:
①盐酸溶解Al2O3薄膜的离子方程式是6H++Al2O3═2Al3++3H2O.
②根据现象Ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
a.浅棕色气体是NO2.
b.实验1的目的是对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能.
c.实验1、2说明反应生成了NO,写出该反应的离子方程式:Al+NO3?+4H+═Al3++NO↑+2H2O.
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在.重新设计实验证实如表:
为确认“刺激性气味”气体,进行如下实验:用湿润KI-淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝. 则:
①刺激性气味的气体是NH3.
②产生该气体的离子方程式是8Al+3NO3-+5OH-+2H2O═3NH3↑+8AlO2-.
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成.实验结果证实:NO3?在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物.因此无色溶液一定能大量存在的是K+、OH-.
(1)加入铝粉产生H2,说明铝具有还原性(填“氧化性”或“还原性”).
(2)甲同学分析:若H+大量存在,则NO3-就不能大量存在.设计实验证实如表:
| 装 置 | 现 象 |
 | Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,液面上方呈浅棕色 Ⅲ.试管变热,溶液沸腾 |
②根据现象Ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
| 实 验 | 内 容 | 现 象 |
| 实验1 | 将湿润KI-淀粉试纸置于空气中 | 未变蓝 |
| 实验2 | 用湿润KI-淀粉试纸检验浅棕色气体 | 试纸变蓝 |
b.实验1的目的是对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能.
c.实验1、2说明反应生成了NO,写出该反应的离子方程式:Al+NO3?+4H+═Al3++NO↑+2H2O.
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在.重新设计实验证实如表:
| 装置 | 现象 |
 | Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,有刺激性气味 |
①刺激性气味的气体是NH3.
②产生该气体的离子方程式是8Al+3NO3-+5OH-+2H2O═3NH3↑+8AlO2-.
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成.实验结果证实:NO3?在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物.因此无色溶液一定能大量存在的是K+、OH-.
8.有A、B、C、D四种金属,分别把它们加入到稀盐酸中,A、B、D反应后有气体放出,C无明显现象,再把A、D加入B盐溶液中,D表面有B析出,而A没有,则四种金属的活动性顺序是为( )
| A. | A>B>D>C | B. | B>D>A>C | C. | D>B>A>C | D. | D>A>B>C |
6.“神舟七号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池.该电池可同时供应电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾.已知该电池的总反应为2H2+O2═2H2O,负极反应为H2+CO${\;}_{3}^{2-}$→CO2↑+H2O+2e-,则下列推断中,正确的是( )
| A. | 通氧气的电极为阳极,发生氧化反应 | |
| B. | 电池放电时,外电路电子由通氧气的正极流向通氢气的负极 | |
| C. | 正极的电极反应为:4OH-→O2↑+2H2O+2e- | |
| D. | 电池工作时,CO${\;}_{3}^{2-}$向负极移动 |
 .
.