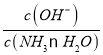题目内容
【题目】无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用。
(1)Nierite是一种高熔点高硬度的陶瓷材料。Nierite的摩尔质量为140 g/mol,其中硅元素的质量分数为60%。已知1 mol NH3与足量的SiCl4充分反应后可得到35 g Nierite与3 mol HCl气体。Nierite的化学式为___________。
(2)K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属。为测定某18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,固体全部溶解后,收集到NO2和N2O4的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O2混合后缓缓通入水中,恰好被完全吸收。
填写该18K金的成分表(精确至0.01%,若不含该金属则填0)。
18K金成分 | Au | Ag |
含量(质量分数) | 75.00% | _________ |
【答案】Si3N4 11.44%
【解析】
(1)确定Nierite有硅元素和氮元素,化学式中硅原子的个数为140×60%÷28=3,氮原子个数为140×40%÷14=4;
(2)设K金中含有铜银两种金属,则根据质量关系列等式为64n(Cu)+108n(Ag)=2.832×(1-75%),金与浓硝酸不反应,铜银与浓硝酸发生氧化还原反应,将HNO3还原为NO2和N2O4,NO2和N2O4的混合气与标准状况下84mLO2混合通入水中恰好被完全吸收获得HNO3,根据电子守恒,即Cu、Ag失去的电子总数等于O2得到的电子总数,2n(Cu)+n(Ag)= ![]() ,联立方程可以求出Ag的质量分数。
,联立方程可以求出Ag的质量分数。
(1)1 mol NH3与足量的SiCl4充分反应后可得到35 g Nierite与3 mol HCl气体,参与反应的SiCl4物质的量为(35g+3mol×36.5g/mol-1mol×17g/mol)÷170g/mol=0.75mol;则Nierite中有硅元素和氮元素,化学式中硅原子的个数为140×60%÷28=3,氮原子个数为140×40%÷14=4,故化学式为Si3N4;
(2)设K金中含有铜银两种金属,则根据质量关系列等式为64n(Cu)+108n(Ag)=2.832×(1-75%),金与浓硝酸不反应,铜银与浓硝酸发生氧化还原反应,将HNO3还原为NO2和N2O4,NO2和N2O4的混合气与标准状况下84mLO2混合通入水中恰好被完全吸收获得HNO3,根据电子守恒,即Cu、Ag失去的电子总数等于O2得到的电子总数,2n(Cu)+n(Ag)= ![]() ,二者联立解得n(Cu)=0.006mol,n(Ag)=0.003mol,Ag的质量分数为
,二者联立解得n(Cu)=0.006mol,n(Ag)=0.003mol,Ag的质量分数为![]() =11.44%,Cu的质量分数为25%-11.44%=13.56%。
=11.44%,Cu的质量分数为25%-11.44%=13.56%。