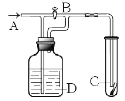
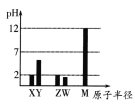
��Ŀ����
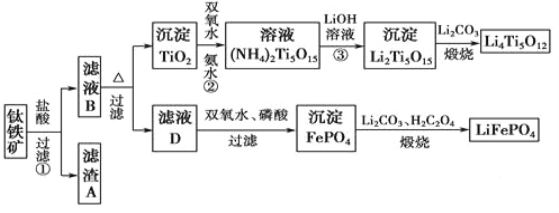
����Ŀ����.��ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+���ӹ�ҵ��ˮ�л������������ͽ���ͭ�Ĺ���������ͼ��ʾ��
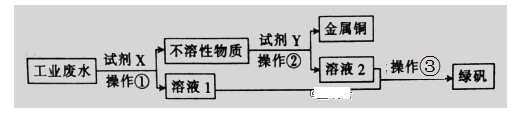
��1�������۵�����Ϊ__________ ��
��2���Լ�XΪ__________���ѧʽ�����������漰�����ӷ�Ӧ����ʽΪ__________ ��
��3���о����������ֺ���Ʒ��Ϻ��з��ĵ�õȣ����ں���+5 ���飨As��Ԫ�أ����������������ģ���˪�ijɷ��� As2O3�����綾���ʣ�ר���Ҹ棺�Է�ʱ��Ҫͬʱ����ʳ�ú��ʺ���ˣ����������ж�����������һ����ʽ����������+����ά���� C=��˪����ʹ���ж�������ά���� C ��________��������������������ԭ����
��4����֪ij��Ӧ�з�Ӧ����������У�KMnO4��H2SO4��MnSO4��H2C2O4��K2SO4��H2O��һ��δ֪��X��
����0.5 molH2C2O4�ڷ�Ӧ��ʧȥ1 mol��������X����X�Ļ�ѧʽΪ__________ ��
�ڽ��������ͻ�ԭ������ƽ��ϵ���������з����У����õ����ű������ת�Ƶķ���� ��Ŀ��__________
![]()
������֪H2C2O4Ϊ���ᣬ��д���÷�Ӧ�����ӷ���ʽ��__________
���𰸡���ȴ�ᾧ Fe Fe + 2H+ = Fe2+ + H2�� ��ԭ�� CO2 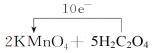 2 MnO4- +5 H2C2O4+6H+ = 2Mn2+ +10 CO2��+8H2O
2 MnO4- +5 H2C2O4+6H+ = 2Mn2+ +10 CO2��+8H2O
��������
��.��ҵ��ˮ�м�����������ۣ�����Cu2+��Ӧ���û���Cu��ʣ����ҺΪ����������Һ���ᾧ��ɵ��̷���
��3������Ʒ���ں���+5 ���飬�븻��ά���� C��ʳ��ͬʳ���ɷ���������ԭ��Ӧ��ά����C�ɽ�+5�۵��黹ԭΪ+3�ۣ�
��4����Ӧ��H2C2O4ʧȥ���ӣ�����CԪ�ػ��ϼ۴�+3�����ߵ�+4�ۣ�����Ӧ���֪X�к���CԪ�أ��һ��ϼ�Ϊ+4�ۣ�������ԭ��Ӧ��MnԪ�ػ��ϼ۽��ͣ���˸�������ԭ��Ӧ�ķ�Ӧ��ΪKMnO4��H2SO4��H2C2O4��������ΪMnSO4��K2SO4��H2O��һ��δ֪��X�����ݻ��ϼ������غ㡢ԭ���غ��д����Ӧ����ʽΪ��2KMnO4 +5 H2C2O4+3H2SO4 = 2MnSO4 +10 CO2��+8H2O���ݴ˷�������
��.��1���ɷ�����֪������Ϊ��ȴ�ᾧ��
��2���Լ�XΪ���ۣ������ķ�ӦΪFe+Cu2+=Cu+Fe2+����������������ϡ���ᷴӦ���ɵõ�����������Һ����˲����ڵķ�ӦΪFe + 2H+ = Fe2+ + H2����
��3��ά����C�ɽ�+5�۵��黹ԭΪ+3�ۣ��ڷ�Ӧ������ԭ����
��4���ٸ��ݷ�����֪X�Ļ�ѧʽΪCO2��
�ڸ÷�Ӧ����������KMnO4����ԭ����H2C2O4�������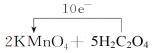 ��
��
�۷�Ӧ����ʽΪ��2KMnO4 +5 H2C2O4+3H2SO4 = 2MnSO4 +10 CO2��+8H2O�������ӷ���ʽΪ��2MnO4- +5H2C2O4+6H+ = 2Mn2+ +10 CO2��+8H2O��

 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�