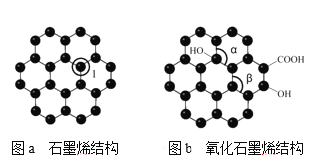
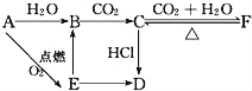
题目内容
【题目】烟道气的主要成分为粉尘、空气、H2O、NOx,其中NOx是主要的大气污染物之一,为了监测某工厂烟道气中NOx含量,采集标准状况下50.00 L烟道气样经除尘、干燥后缓慢通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3,除去多余的H2O2并加水稀释至100.00 mL。量取20.00 mL该溶液,加入30.00 mL 0.01000 mol·L1FeSO4标准溶液(过量),充分反应后,用0.001000 mol·L1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00 mL。滴定过程中发生如下反应:
Fe2+ + NO3 + H+ — NO↑ + Fe3+ + H2O (未配平)
![]() + Fe2+ + H+ — Cr3+ + Fe3++ H2O (未配平)
+ Fe2+ + H+ — Cr3+ + Fe3++ H2O (未配平)
(1)NO被H2O2氧化为NO3的离子方程式是_________。
(2)配制100mL 0.001000 mol·L1 K2Cr2O7标准溶液时,除需用到烧杯、量筒、玻璃棒外,还需用到的玻璃仪器有_________、_________。
(3)若FeSO4标准溶液部分变质,会使NOx含量测定结果_________(填“偏高” 、“偏低”或“无影响 ”)。
(4)标准状况下该工厂烟道气中NOx(折合成NO2)的含量为_________mg·m3(写出计算过程)。
【答案】2NO+3H2O2=2H++2NO![]() +2H2O 胶头滴管 100mL容量瓶 偏高 368 mg·m3
+2H2O 胶头滴管 100mL容量瓶 偏高 368 mg·m3
【解析】
(1)NO被H2O2氧化为NO3,H2O2被还原为H2O,据此写出反应的离子方程式;
(2)配制一定浓度的溶液,需用到烧杯、量筒、玻璃棒、胶头滴管、100mL容量瓶,据此进行解答。
(3)若FeSO4标准溶液部分变质,则消耗K2Cr2O7溶液的体积减小,计算时求得NO3-的物质的量增大,会使NOx含量测定结果偏高;
(4)根据![]() +6 Fe2+ + 14H+ =2Cr3+ + 6Fe3++7 H2O、3Fe2+ + NO3 + 4H+ = NO↑ + 3Fe3+ +2 H2O反应中各量之间的关系进行计算。
+6 Fe2+ + 14H+ =2Cr3+ + 6Fe3++7 H2O、3Fe2+ + NO3 + 4H+ = NO↑ + 3Fe3+ +2 H2O反应中各量之间的关系进行计算。
(1)NO被H2O2氧化为NO3,H2O2被还原为H2O,反应的离子方程式是2NO+3H2O2=2H++2NO![]() +2H2O;
+2H2O;
答案为:2NO+3H2O2=2H++2NO![]() +2H2O;
+2H2O;
(2)配制100mL 0.001000 mol·L1 K2Cr2O7标准溶液时,除需用到烧杯、量筒、玻璃棒外,还需用到的玻璃仪器有胶头滴管、100mL容量瓶;
答案为:胶头滴管、100mL容量瓶;
(3)若FeSO4标准溶液部分变质,则消耗K2Cr2O7溶液的体积减小,计算时求得NO3-的物质的量增大,会使NOx含量测定结果偏高;
答案为:偏高;
(4)根据反应![]() +6 Fe2+ + 14H+ =2Cr3+ + 6Fe3++7 H2O
+6 Fe2+ + 14H+ =2Cr3+ + 6Fe3++7 H2O
1mol 6mol
5×10-5mol 3×10-4mol
3Fe2+ + NO3 + 4H+ = NO↑ + 3Fe3+ +2 H2O
3mol 1mol
15×10-4mol-3×10-4mol 4×10-4mol
标准状况下该工厂烟道气中NOx(折合成NO2)的含量为![]() =368mg·m3;
=368mg·m3;
答案为:368。