题目内容
15.同温同压下,33g气体X的体积与24g O2的体积相同,则X为( )| A. | CH4 | B. | CO | C. | CO2 | D. | SO2 |
分析 同温同压下,33g气体X和24gO2 所占体积相同,则二者的物质的量相同,根据n=$\frac{m}{M}$计算氧气的物质的量,根据M=$\frac{m}{n}$计算气体X的摩尔质量,结合选项判断气体X的可能化学式.
解答 解:24gO2 的物质的量为$\frac{24g}{32g/mol}$=0.75mol,同温同压下,33g气体X和24gO2 所占体积相同,则二者的物质的量相同,所以气体X的摩尔质量为$\frac{33g}{0.75mol}$=44g/mol,
CH4的摩尔质量为16g/mol,CO的摩尔质量为28g/mol,CO2的摩尔质量为44g/mol,SO2的摩尔质量为64g/mol,故X为CO2,
故选C.
点评 本题考查物质的量计算、阿伏伽德罗定律及推论,侧重分析能力及计算能力的考查,题目难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
5.化学与生产、生活、环境密切相关.下列有关说法正确的是( )
| A. | 乙烯在氧气中燃烧时放出热量,因此常用它来焊接或切割金属 | |
| B. | 乙二醇和丙三醇都是无色、黏稠、有甜味的液体,常用于配制化妆品 | |
| C. | 油脂在碱性条件下水解出的甘油常用于生产肥皂 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
3.一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后,恢复到原来的温度,下列说法中正确的是( )
| A. | 溶液中pH值不变,有H2放出 | B. | 液液中Na+数目减少,有O2放出 | ||
| C. | 溶液中pH值增大,有O2放出 | D. | 溶液中Na+浓度增大,有O2放出 |
20.等温等容条件下有反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径建立平衡.Ⅰ:A、B的起始浓度均为2mol/L;Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L.下列叙述正确的是( )
| A. | Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成相同 | |
| B. | Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成不同 | |
| C. | 达到平衡时Ⅰ途径的vA等于Ⅱ途径的vA | |
| D. | 达到平衡后,第Ⅰ途径混合气密度为第Ⅱ途径混合气密度的$\frac{1}{2}$ |
7.下列离子方程式书写正确的是( )
| A. | Cu(OH)2浊液中滴加醋酸:Cu(OH)2+2H+═Cu2++2H2O | |
| B. | NaOH溶液中加入铝片:2Al+2 OHˉ═2AlO2ˉ+3H2↑ | |
| C. | 已知Fe2+可以还原C12、Br2,C12可以氧化Br-生成Br2,在标准状况下,向10mL 0.1moL/LFeBr2溶液中通入22.4mL氯气:2Fe2++2Br-+2C12═2Fe3++Br2+4C1- | |
| D. | NaHCO3溶液与稀硫酸溶液的反应:HCO3-+H+═H2O+CO2↑ |
4.下列说法正确的是( )
| A. | C4H10和C20H42 互为同系物 | B. | 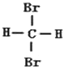 和 和 互为同分异构体 | ||
| C. | 12C和14C互为同素异形体 | D. | H2、D2和T2互为同位素 |
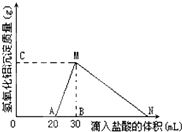 在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示.问:
在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示.问: