题目内容
【题目】下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为3﹕1的是( )
A.对二甲苯
B.乙酸乙酯
C.乙醛
D.苯
【答案】C
【解析】
在核磁共振氢谱中能出现两组峰,说明该分子中含有两类氢原子,且其峰面积之比为3:1,说明这两类氢原子的个数比是3:1。
A.对二甲苯的结构简式为:![]() ,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,A错误;
,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,A错误;
B.乙酸乙酯的结构简式为CH3COOCH2CH3,该分子的核磁共振氢谱中有三组峰,其峰面积之比是3:3:2,B错误;
C.乙醛的结构简式为CH3CHO,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:1,C正确;
D.苯的结构简式为![]() ,该分子的核磁共振氢谱中只有一组峰,D错误;
,该分子的核磁共振氢谱中只有一组峰,D错误;
答案选C。

【题目】教材中给出了Na2O2与水反应的化学方程式,某学习小组通过实验研究Na2O2与水发反应机理
操作 | 现象 |
Ⅰ | 剧烈反应,产生的气体能使带火星木条复燃,固体全部溶解后,得到的无色溶液a |
Ⅱ | 溶液变红,10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
Ⅲ | 又有大量气泡产生,产生的气体也能使带火星木条复燃 |
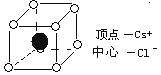
(1)Na2O2的电子式为 ______ ,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表示反应的机理,写出Na218O2与H2O反应的化学方程式 ______ .
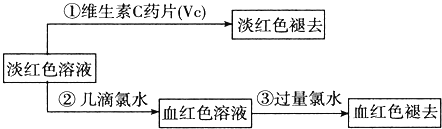
(2)操作Ⅱ中红色褪去的可能原因是 ______ .
(3)用反应![]() 测定溶液a中H2O2含量.取20.00ml溶液a,用稀 ______
测定溶液a中H2O2含量.取20.00ml溶液a,用稀 ______ ![]() 填化学式
填化学式![]() 酸化,用0.002molL-1KMnO4溶液滴定,至终点时平均消耗10.00ml KMnO4溶液.滴定时KMnO4溶液应装在 ______
酸化,用0.002molL-1KMnO4溶液滴定,至终点时平均消耗10.00ml KMnO4溶液.滴定时KMnO4溶液应装在 ______ ![]() 填酸或碱
填酸或碱![]() 式滴定管中,终点确定的方法是 ______ ,经计算溶液a中c(H2O2)= ______ molL-1
式滴定管中,终点确定的方法是 ______ ,经计算溶液a中c(H2O2)= ______ molL-1
(4)向溶液a中滴加FeSO4溶液,发生反应的离子方程式为______ .
(5)向FeSO4溶液中加入一定量Na2O2固体,并以物质的量为2:1发生反应,反应中无气体生成,写出反应的离子方程式 ______ .